AGENT BRAND
品牌專題對(duì)于您的超分辨成像研究,有什么比頂級(jí)質(zhì)量的一抗更好呢?這些一抗經(jīng)世界各地知名研究人員驗(yàn)證,結(jié)合高質(zhì)量染料,專門設(shè)計(jì)以完美滿足STED超分辨顯微鏡的特定要求。在這里,SYSY呈現(xiàn)了在神經(jīng)科學(xué)領(lǐng)域中最廣泛使用的SYSY一抗系列,直接與匹配的abberior STAR染料偶聯(lián),經(jīng)過(guò)優(yōu)化以適用于STED顯微鏡。
簡(jiǎn)介
揭示突觸的結(jié)構(gòu)和功能長(zhǎng)期以來(lái)取得了成功。然而,傳統(tǒng)顯微技術(shù)中的衍射限制了分辨率,從而限制了對(duì)突觸結(jié)構(gòu)和功能的洞察。超分辨顯微鏡技術(shù)實(shí)現(xiàn)了前所未有的精度,可以可視化突觸結(jié)構(gòu)。這種能力轉(zhuǎn)變了我們檢查突觸間隙、活躍區(qū)和 postsynaptic 密度內(nèi)蛋白質(zhì)的空間組織的能力,可以極為詳細(xì)地展示。它促進(jìn)了對(duì)分子水平上突觸組分的異質(zhì)性和動(dòng)態(tài)性的研究。
|
|
| Figure 1A: 用abberior STAR RED標(biāo)記的突觸前巴松管和用abberior星星橙子標(biāo)記的突觸后Homer 1使用STED顯微鏡顯示分離良好的突觸結(jié)構(gòu)。 | Figure 1B: 巴松管和Homer 1的突觸定位示意圖。 |
神經(jīng)遞質(zhì)/化學(xué)突觸的結(jié)構(gòu)
神經(jīng)元必須快速而準(zhǔn)確地傳遞信息;它們負(fù)責(zé)從我們身體各個(gè)部位,從腳趾尖到大腦,迅速傳遞信號(hào),然后在大腦中處理這些信息。為了實(shí)現(xiàn)如此快速和精準(zhǔn)的溝通,突觸優(yōu)化其處理高需求和間歇信號(hào)處理的能力。
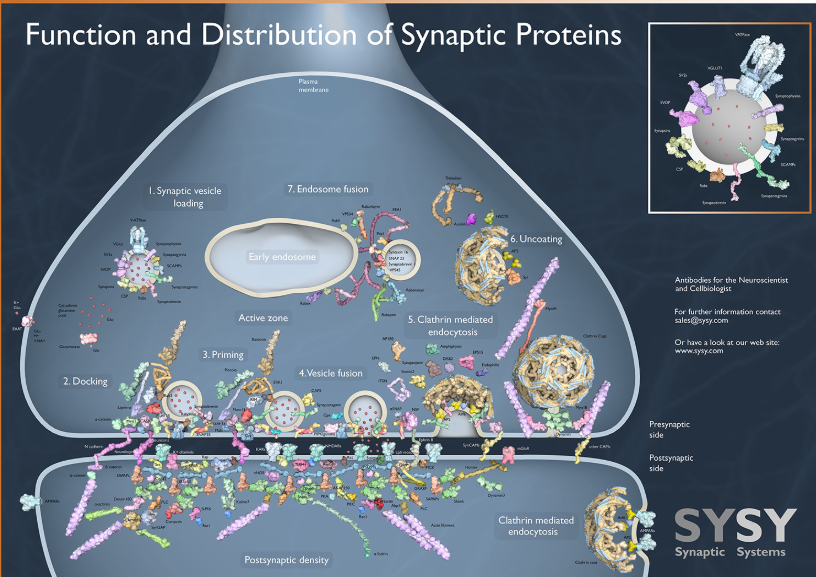
化學(xué)突觸是脊椎動(dòng)物中主要發(fā)現(xiàn)的一種突觸類型,是一個(gè)不連續(xù)的結(jié)構(gòu),由一個(gè)突觸前神經(jīng)元和一個(gè)突觸后神經(jīng)元組成,它們之間被大約15-20納米寬的突觸間隙分隔。化學(xué)突觸中的信號(hào)傳遞是通過(guò)突觸囊循環(huán)進(jìn)行的。突觸囊和活躍區(qū)中發(fā)現(xiàn)的專門蛋白質(zhì)在協(xié)調(diào)突觸囊循環(huán)中起著關(guān)鍵作用。SNARE蛋白,如Syntaxin、Synaptobrevin和SNAP-25,參與了突觸囊與質(zhì)膜的融合。像Bassoon、Piccolo和RIM這樣的支架蛋白組織和招募突觸囊靠近質(zhì)膜。Synapsins通過(guò)與細(xì)胞骨架蛋白結(jié)合幫助突觸囊的移動(dòng),而complexins防止囊泡的自發(fā)融合。此外,CAPS(鈣激活分泌蛋白)促進(jìn)了鈣信號(hào)與突觸囊融合的耦合(Chua等,2010年;Jahn和Fasshauer,2012年)。
突觸后密度(PSD)是一個(gè)富含蛋白質(zhì)的特殊區(qū)域,對(duì)于接收來(lái)自突觸前神經(jīng)元的神經(jīng)遞質(zhì)信號(hào)并啟動(dòng)突觸后反應(yīng)至關(guān)重要。PSD中豐富的是神經(jīng)遞質(zhì)受體,每個(gè)突觸中主要由突觸前神經(jīng)元釋放的神經(jīng)遞質(zhì)決定。這種受體釋放的神經(jīng)遞質(zhì)配對(duì)決定了每個(gè)特定突觸的電學(xué)特性。此外,各類支架蛋白,如PSD-95、Shank和Homer,在錨定和組織信號(hào)分子、受體和結(jié)構(gòu)蛋白在突觸后密度中發(fā)揮關(guān)鍵作用(Takamori等,2006年;Chua等,2010年)。
突觸間隙主要充滿細(xì)胞外基質(zhì)和其他非蛋白成分。其中包括細(xì)胞粘附分子,如cadherins、integrins、neuroligins(存在于突觸后膜中)和neurexins(存在于突觸前膜中)。它們共同介導(dǎo)突觸粘附,并在突觸形成和功能中發(fā)揮作用。額外的細(xì)胞外基質(zhì)蛋白如laminins、collagens和proteoglycans有助于組織和穩(wěn)定突觸連接(Dankovich和Rizzoli,2022年)。
顯微鏡技術(shù)的進(jìn)步,特別是超分辨技術(shù),使我們能夠以驚人的細(xì)節(jié)觀察突觸。這些技術(shù)使科學(xué)家能夠觀察特定蛋白質(zhì)相互作用以及突觸和突觸囊的異質(zhì)性,大大加深了我們對(duì)這些復(fù)雜生物結(jié)構(gòu)的理解(Binotti等,2024年;Upmanyu等,2022年;Nishimune等,2016年;Willig等,2006年)。然而,許多突觸結(jié)構(gòu)和功能方面仍未解決。例如,前突觸活躍區(qū)(AZ)的精細(xì)結(jié)構(gòu),分子簇的重要性以及突觸囊循環(huán)背后的動(dòng)態(tài)和分子機(jī)制仍未完全描述(Nosov等,2020年)。
STED顯微鏡
在納米級(jí)光顯微鏡技術(shù)出現(xiàn)之前,特別是STED(受激發(fā)射消融)顯微鏡技術(shù)的發(fā)展之前,研究人員受到傳統(tǒng)光顯微鏡的衍射限制。這個(gè)限制將分辨率限制在大約200-300納米橫向和約500-700納米軸向。STED顯微鏡的概念由Stefan Hell和Jan Wichmann于1994年提出,并于2000年進(jìn)行了實(shí)驗(yàn)驗(yàn)證(Hell和Wichmann,1994年,Klar等,2000年)。STED顯微鏡基于傳統(tǒng)共焦激光掃描配置,但除了一個(gè)激發(fā)激光外,還包括一個(gè)第二個(gè)紅移和環(huán)形STED激光,其中心為零強(qiáng)度。這樣,除了環(huán)形中心的分子外,所有分子都被消融。這種配置確保了由中央光束激發(fā)的熒光分子會(huì)被STED光束迅速去激發(fā),而來(lái)自STED環(huán)形中心的任何熒光則得以保留。熒光信號(hào)被銳化,達(dá)到了30-70納米的橫向分辨率。衍射屏障被突破。
成功進(jìn)行STED成像的先決條件
良好的成像結(jié)果取決于兩個(gè)條件:良好的熒光染料和特異性抗體。用于STED的理想熒光探針必須具備幾個(gè)關(guān)鍵屬性:對(duì)STED光束的響應(yīng)以實(shí)現(xiàn)高效去激發(fā)、優(yōu)化的吸收和發(fā)射光譜與STED系統(tǒng)中可用的激光線匹配、在反復(fù)激發(fā)和去激發(fā)循環(huán)中耐光漂白。為了實(shí)現(xiàn)最佳的STED成像效果,STED染料的先驅(qū)公司abberior提供了經(jīng)過(guò)特別優(yōu)化的熒光染料。以其卓越的光穩(wěn)定性、定制的光譜特性、高效的去激發(fā)能力、高量子產(chǎn)額、與生物樣品兼容性以及最小的背景噪音而聞名,abberior STAR ORANGE和STAR RED是775納米雙色STED的完美組合。 在STED顯微鏡中實(shí)現(xiàn)高空間分辨率,所使用的用于染色活體或固定樣本的抗體的選擇至關(guān)重要。SYSY抗體具有高特異性和親和力,使其成為您顯微鏡分析的精確而強(qiáng)大的工具。使用經(jīng)過(guò)充分表征的單克隆抗體,具有高特異性結(jié)合到單一抗原表位,可以減少染色模式的變異性,減少與其他蛋白質(zhì)或分子的交叉反應(yīng)的可能性。
直接偶聯(lián)的優(yōu)勢(shì)
與使用標(biāo)記的二抗間接標(biāo)記相比,直接偶聯(lián)顯示出一系列重大優(yōu)勢(shì)。除了消除對(duì)二抗的需求外,直接偶聯(lián)還減少了空間位阻,這在間接標(biāo)記中可能降低了一抗對(duì)靶標(biāo)的親和力和特異性。此外,通過(guò)減少非特異性二級(jí)結(jié)合到非靶蛋白(交叉反應(yīng))的背景噪音,減少了熒光團(tuán)與抗原之間的距離,并防止多個(gè)二級(jí)抗體結(jié)合到單個(gè)一級(jí)抗體而掩蓋單個(gè)分子的空間排列(Früh等,2021年)。
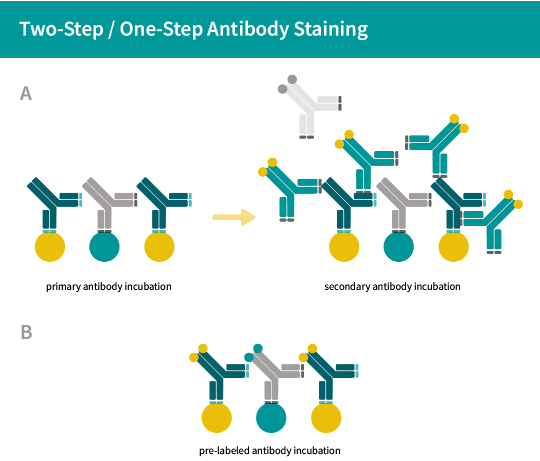
Figure 3: 一抗的直接偶聯(lián)(一步,B)減少了空間位阻、熒光團(tuán)距離和表位掩蔽,這可能使用耗時(shí)的二抗兩步染色(A)發(fā)生。
使用與abberior STAR染料結(jié)合的SYSY原代抗體,進(jìn)一步提升您的STED顯微鏡體驗(yàn)。
SYSY抗體符合STED超分辨顯微鏡的特定要求。
| 貨號(hào) | 產(chǎn)品名稱 | 應(yīng)用 | 規(guī)格 |
| 141-111AbOR | Bassoon, mouse, monoclonal, purified IgG, AbberiorStar ORANGE K.O. | ICC | 100 ?g |
| 141-111AbRED | Bassoon, mouse, monoclonal, purified IgG, AbberiorStar RED K.O. | ICC | 100 ?g |
| 160-111AbOR | Homer1b/c, mouse, monoclonal, purified IgG, AbberiorStar ORANGE | ICC | 100 ?g |
| 160-111AbRED | Homer1b/c, mouse, monoclonal, purified IgG, AbberiorStar RED | ICC | 100 ?g |
| 162-311AbOR | Shank3, mouse, monoclonal, purified IgG, AbberiorStar ORANGE | ICC | 100 ?g |
| 162-311AbRED | Shank3, mouse, monoclonal, purified IgG, AbberiorStar RED | ICC | 100 ?g |
| 106-011AbOR | Synapsin1, mouse, monoclonal, purified IgG, AbberiorStar ORANGE K.O. | ICC | 100 ?g |
| 106-011AbRED | Synapsin1, mouse, monoclonal, purified IgG, AbberiorStar RED K.O. | ICC | 100 ?g |
| 104 211AbOR | Synaptobrevin2, mouse, monoclonal, purified IgG, AbberiorStar ORANGE K.O. K.D. | ICC | 50 ?g |
| 104-211AbRED | Synaptobrevin2, mouse, monoclonal, purified IgG, AbberiorStar RED K.O. K.D. | ICC | 50 ?g |
| 101-011AbOR | Synaptophysin1, mouse, monoclonal, purified IgG, AbberiorStar ORANGE K.O. K.D. | ICC | 50 ?g |
| 101-011AbRED | Synaptophysin1, mouse, monoclonal, purified IgG, AbberiorStar RED K.O. K.D. | ICC | 50 ?g |
| 105-011AbOR | Synaptotagmin1, mouse, monoclonal, purified IgG, AbberiorStar ORANGE K.O. K.D. | ICC | 100 ?g |
| 105-011AbRED | Synaptotagmin1, mouse, monoclonal, purified IgG, AbberiorStar RED K.O. K.D. | ICC | 100 ?g |
引用:
Binotti et al., 2024: ATG9 resides on a unique population of small vesicles in presynaptic nerve terminals. PMID: 37881948
Chua et al., 2010: The architecture of an excitatory synapse. PMID: 20200227
Dankovich and Rizzoli, 2022: The Synaptic Extracellular Matrix: Long-Lived, Stable, and Still Remarkably Dynamic. PMID: 35350469
Früh et al., 2021: Site-Specifically-Labeled Antibodies for Super-Resolution Microscopy Reveal In Situ Linkage Errors. PMID: 34184536
Hell and Wichmann, 1994: Breaking the diffraction resolution limit by stimulated emission: stimulated-emission-depletion fluorescence microscopy. PMID: 19844443
Jahn and Fasshauer 2012: Molecular machines governing exocytosis of synaptic vesicles. PMID: 23060190
Klar et al., 2000: Fluorescence microscopy with diffraction resolution barrier broken by stimulated emission. PMID: 10899992
Nishimune et al., 2016: Dual-color STED microscopy reveals a sandwich structure of Bassoon and Piccolo in active zones of adult and aged mice. PMID: 27321892
Nosov et al., 2020: The Decade of Super-Resolution Microscopy of the Presynapse. PMID: 32848695
Takamori et al., 2006: Molecular anatomy of a trafficking organelle. PMID: 17110340
Upmanyu et al., 2022: Colocalization of different neurotransmitter transporters on synaptic vesicles is sparse except for VGLUT1 and ZnT3. PMID: 35263617
Willig et al., 2006: STED microscopy reveals that synaptotagmin remains clustered after synaptic vesicle exocytosis. PMID: 16612384

微信掃碼在線客服