PRODUCT CENTER
特色產品隨著干細胞治療應用的增長,對其移植后體內檢測方法的開發(fā)和完善需求也在增加。磁共振成像已成為追蹤移植干細胞的主要方式之一。MRI的優(yōu)勢在于它是一種非侵入性方法,不沉積電離能量,適合進行縱向研究。為了使用MRI區(qū)分特定細胞,這些細胞必須用磁性對比劑進行標記。目前,最徹底表征的試劑,F(xiàn)eridex,一種FDA批準的用于肝臟成像的超順磁性氧化鐵(SPIO)對比劑,已不再可用。來自Biopal的Molday ION Rhodamine-B TM(MIRB)是一種新型SPIO對比劑,專為細胞標記應用而配制。MIRB的磁性核心和流體動力學尺寸分別大約為8和35納米,Zeta值為-31毫伏,與Rhodamine-B(Rh-B)(每個顆粒2個熒光體)結合,可以通過MRI和熒光顯微鏡觀察。Rh-B的激發(fā)波長為555納米,發(fā)射波長為565-620納米。在這項研究中,我們定性和定量地表征了MIRB在非人靈長類動物(NHP)間充質干細胞(MSC)上的標記和裝載特性,包括在不同標記濃度下的平均內部鐵/MSC,以及細胞內MIRB對MSC活性、增殖能力和功能的影響。我們對MIRB標記的MSC的體外MR特性進行了全面評估,描述了弛豫率測量、最佳成像序列的確定以及在臨床1.5 T西門子交響曲MRI設備上的理想檢測極限。這些研究為新的SPIO對比劑用于細胞標記和體內MRI檢測的未來應用奠定了基礎,并提供了原理證明。
艾美捷Molday ION羅丹明B熒光標記物(BPL-CL-50Q02-6A-50)部分結果分析:
1 細胞標記和裝載特性分析
1.1 細胞內MIRB分布
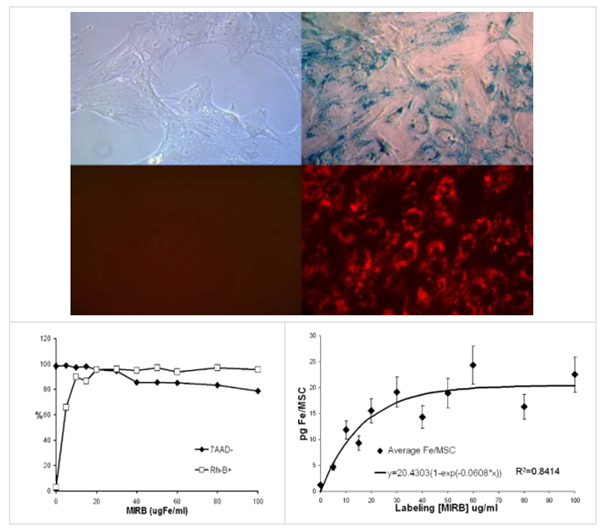
經過20小時的孵化,觀察到內化的MIRB定位在MSC的細胞質中,特別是在核周體的內吞體中。這種定位模式在光學和熒光顯微鏡下都很明顯,并且適用于所有考慮的標記條件。圖1顯示了通過普魯士藍染色增強的光顯微鏡圖像,用于鐵(Fe)的可視化,以及MSC細胞質中Rh-B的熒光顯微鏡圖像。
1.2 標記效率
標記效率,通過流式細胞儀檢測Rh-B陽性細胞的百分比,對于用5 mg Fe/ml標記的細胞范圍從65.9%,對于用MIRB濃度達到或超過20 mg Fe/ml標記的細胞則超過95%。圖2顯示了在高達100 mg Fe/ml的MIRB濃度下標記的MSC中Rh-B存在的流式細胞術數(shù)據(jù)。
1.3 MIRB攝取量
平均每MSC中內化的MIRB量,以pg Fe計,如圖3所示。平均Fe/MSC的計算是手動在血細胞計數(shù)板上進行的細胞計數(shù)的直接函數(shù)。手動細胞計數(shù)引入的誤差,估計在10-15%(37),代表了主要誤差以及細胞內鐵含量估算的準確性限制。來自六項檢測的數(shù)據(jù)表明,隨著MIRB標記濃度的增加,出現(xiàn)了飽和現(xiàn)象。在20至30 mg Fe/ml之間的標記濃度達到平臺期,結果平均每MSC攝取量約為15-20 pg Fe。
Molday ION羅丹明B熒光標記物部分文獻參考:
1. Budde MD, Frank JA. Magnetic tagging of therapeutic cells forMRI. J Null Med 2009; 50(2): 171–174.
2. Adler ED, Bystrup A, Briley-Saebo KC, Mani V, Young W, Giovanonne S, Altman P, Kattman SJ, Frank JA, Weinmann HJ, KellerGM, Fayad ZA. In vivo detection of embryonic stem cell-derivedcardiovascular progenitor cells using Cy3-labeled Gadofluorine Min murine myocardium. JACC Cardiovasc Imag 2009; 2(9):1114–1122.
3. Brekke C, Williams SC, Price J, Thorsen F, Modo M. Cellularmultiparametric MRI of neural stem cell therapy in a rat gliomamodel. Neuroimage 2007; 37(3): 769–782.
4. Guzman R, Uchida N, Bliss TM, He D, Christopherson KK, Stellwagen D, Capela A, Greve J, Malenka RC, Moseley ME, Palmer TD,Steinberg GK. Long-term monitoring of transplanted humanneural stem cells in developmental and pathological contextswith MRI. Proc Natl Acad Sci USA 2007; 104(24): 10211–10216.
5. Higuchi T, Anton M, Dumler K, Seidl S, Pelisek J, Saraste A, WellingA, Hofmann F, Oostendorp RA, Gansbacher B, Nekolla SG, BengelFM, Botnar RM, Schwaiger M. Combined reporter gene PET andiron oxide MRI for monitoring survival and localization of transplanted cells in the rat heart. J Nucl Med 2009; 50(7): 1088–1094.
6. Onda T, Honmou O, Harada K, Houkin K, Hamada H, Kocsis J.D.Therapeutic benefits by human mesenchymal stem cells (hMSCs)and Ang-1 gene-modified hMSCs after cerebral ischemia. J CerebBlood Flow Metab 2008; 28(2): 329–340.
7. Chang NK, Jeong YY, Park JS, Jeong HS, Jang S, Jang MJ, Lee JH,Shin SS, Yoon W, Chung TW, Kang HK. Tracking of neural stemcells in rats with intracerebral hemorrhage by the use of 3T MRI.Korean J Radiol 2008; 9(3): 196–204.
8. Dousset V, Tourdias T, Brochet B, Boiziau C, Petry KG. How to tracestem cells for MRI evaluation? J Neurol Sci 2008; 265(1–2):122–126.

微信掃碼在線客服