PRODUCT CENTER
特色產(chǎn)品當(dāng)前位置:首頁(yè) > 特色產(chǎn)品
【應(yīng)用】
Aquarray, Leopoldshafen, Germany

TheWell Bioscience, North Brunswick, NJ 08902

【液滴微陣列平臺(tái)】
液滴微陣列(DMA)由超疏水背景上的親水點(diǎn)組成,允許在平面表面上形成亞微升范圍內(nèi)分離且均勻的液滴。使用納升液體分配器精確填充通常尺寸為350 - 1000 ?m的DMA斑點(diǎn)。每個(gè)DMA具有672 - 6048個(gè)液滴的容量,使得在DMA平臺(tái)上能夠進(jìn)行高度微型化的高通量篩選。
圖1. 具有672個(gè)1mm大小斑點(diǎn)的液滴微陣列,每滴分配150nL。
DMA已被用于多種化學(xué)和生物應(yīng)用,包括芯片上的高通量化學(xué)合成及隨后的生物篩選(1)、基于轉(zhuǎn)染的篩選(2)、斑馬魚(yú)胚胎篩選(3)、細(xì)菌篩選(4)和基于細(xì)胞的化合物篩選。細(xì)胞篩選可以使用任何細(xì)胞類(lèi)型進(jìn)行,例如細(xì)胞系、干細(xì)胞或原代細(xì)胞,在貼壁或懸浮培養(yǎng)中,使用基于球體的細(xì)胞培養(yǎng)模型進(jìn)行2D或3D培養(yǎng)。使用懸滴技術(shù)在含有150個(gè)細(xì)胞的100nL液滴中,在24 - 48小時(shí)內(nèi)已證明在不同的腫瘤細(xì)胞系中形成單個(gè)球體(6)。
【VitroGel 水凝膠平臺(tái)】
VitroGel無(wú)外源成分(無(wú)動(dòng)物源)水凝膠系統(tǒng)是動(dòng)物源性細(xì)胞外基質(zhì)(ECM)的Z越替代品,避免了未知成分的不確定性,為獲得一致的結(jié)果,提供了明確且具有生物學(xué)功能的微環(huán)境。該水凝膠在室溫下具有獨(dú)特的流變剪切稀化和快速恢復(fù)特性,允許高通量分配的極其順暢的過(guò)程,并為微陣列應(yīng)用提供出色的水凝膠液滴均勻性。
本應(yīng)用筆記重點(diǎn)介紹了使用即用型、無(wú)外源成分的功能性水凝膠系統(tǒng)VitroGel 水凝膠基質(zhì)(VHM01)在DMA上生成腫瘤細(xì)胞球體。該水凝膠在室溫下穩(wěn)定,pH值中性,透明,可滲透液體/營(yíng)養(yǎng)物質(zhì),并經(jīng)過(guò)優(yōu)化以支持多種細(xì)胞類(lèi)型。與細(xì)胞培養(yǎng)基混合后,形成柔軟可注射的水凝膠,非常適合本研究中的注射或液體分配。
由于納升體積和斑點(diǎn)之間的差距較小,在微型DMA平臺(tái)上進(jìn)行分配對(duì)液體分配器來(lái)說(shuō)具有挑戰(zhàn)性。已經(jīng)確定了許多能夠準(zhǔn)確瞄準(zhǔn)DMA上斑點(diǎn)的非接觸式液體分配器。此外,由于水凝膠的高粘度,其分配可能具有挑戰(zhàn)性。然而,由于其獨(dú)特的流變特性,VitroGel可以在室溫或37°C下保持長(zhǎng)期(數(shù)小時(shí))可注射狀態(tài),而不會(huì)堵塞分配器的源孔。將150nL的VitroGel -細(xì)胞混合物分配到具有672個(gè)斑點(diǎn)的DMA上大約需要一分鐘,并產(chǎn)生非常均勻的模式。人宮頸癌細(xì)胞系HeLa和人黑色素瘤細(xì)胞系SK - MEL - 28在培養(yǎng)72小時(shí)后,在每個(gè)DMA液滴的VitroGel基質(zhì)中形成許多存活的圓形球體(圖2和圖3)。
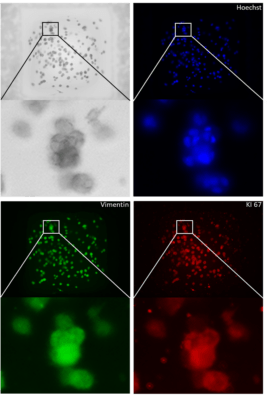
圖2. 通過(guò)在DMA上分配與細(xì)胞混合的VitroGel生成HeLa球體。如材料和方法中所述,72小時(shí)后進(jìn)行針對(duì)波形蛋白(綠色)和KI67(紅色)的免疫熒光染色。細(xì)胞核用Hoechst染色。上圖:一個(gè)斑點(diǎn)的描述。下圖:其放大圖。
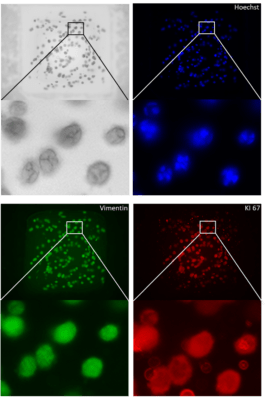
圖3. 通過(guò)在DMA上分配與細(xì)胞混合的VitroGel生成SK - MEL 28球體。如材料和方法中所述,72小時(shí)后進(jìn)行針對(duì)波形蛋白(綠色)和KI67(紅色)的免疫熒光染色。細(xì)胞核用Hoechst染色。
【結(jié)論】
總之,成功地使用即用型、無(wú)外源成分的功能性水凝膠系統(tǒng)VitroGel水凝膠基質(zhì)(VHM01)在DMA上生成了腫瘤細(xì)胞球體。形成了兩種類(lèi)型的腫瘤細(xì)胞球體。通過(guò)免疫熒光染色進(jìn)行了可視化。通過(guò)在DMA上分配與細(xì)胞混合的VitroGel生成HeLa球體。如材料和方法中所述,72小時(shí)后進(jìn)行針對(duì)波形蛋白(綠色)和KI67(紅色)的免疫熒光染色。細(xì)胞核用Hoechst染色。通過(guò)在DMA上分配與細(xì)胞混合的VitroGel生成SK - MEL 28球體。如材料和方法中所述,72小時(shí)后進(jìn)行針對(duì)波形蛋白(綠色)和KI67(紅色)的免疫熒光染色。細(xì)胞核用Hoechst染色。
【材料和方法】
細(xì)胞培養(yǎng)
HeLa和SK - MEL 28細(xì)胞在含有10%胎牛血清(FBS)的Dulbecco改良Eagle培養(yǎng)基(DMEM)中培養(yǎng)。當(dāng)培養(yǎng)物達(dá)到80 - 90%合流時(shí)進(jìn)行傳代。
3D培養(yǎng)
對(duì)于HeLa和SK - MEL 28細(xì)胞的3D培養(yǎng),使用了VitroGel水凝膠基質(zhì)。在含有30%FBS的DMEM培養(yǎng)基中制備細(xì)胞懸液。將400uL的VitroGel溶液與200uL的細(xì)胞懸液以2:1的比例(v / v)混合,以使水凝膠 - 細(xì)胞混合物的最終FBS濃度為10%。
【分配】
使用低體積納升分配器I - DOT Mini(AQ版)將水凝膠 - 細(xì)胞混合物分配到具有672個(gè)1mm大小斑點(diǎn)的液滴微陣列上。將400uL的水凝膠 - 細(xì)胞混合物加載到源孔中,并使用“VitroGel”液體類(lèi)別(4滴253mbar)在66秒內(nèi)進(jìn)行每點(diǎn)150nL的分配。立即將DMA轉(zhuǎn)移到含有4mL加濕緩沖液和蓋子中加濕墊的培養(yǎng)皿中。在室溫下孵育15分鐘后,將50nL含有10%FCS的DMEM分配到每個(gè)液滴上。立即將DMA轉(zhuǎn)移回加濕培養(yǎng)皿中,并在37°C和5%CO2下孵育。
【在液滴微陣列(DMA)上進(jìn)行KI67和波形蛋白的免疫熒光染色和顯微鏡觀察】
在將細(xì)胞接種到DMA上72小時(shí)后進(jìn)行染色。將DMA在適當(dāng)?shù)娜旧萜髦薪氡涞腜BS中洗滌三次。在染色容器中,用4%福爾馬林在室溫下固定細(xì)胞,然后用TBS(3X)洗滌。然后將DMA在含有0.1%Triton X - 100的TBS(9.9ml TBS + 100uL Triton X - 100)中在染色罐中孵育15分鐘,然后進(jìn)行三次洗滌步驟。為了減少非特異性結(jié)合,將DMA直接在DMA上與Power Block(在dd H2O中1:10稀釋?zhuān)┮黄鸱跤⑹褂檬災(zāi)ば⌒牡胤植荚谡麄€(gè)DMA上。用真空除去任何剩余的液體。 最后,將150nL的一抗混合物(在最大75bar下)分配到DMA的每個(gè)斑點(diǎn)上,并在濕潤(rùn)室中在4°C下孵育過(guò)夜(KI67多克隆抗體:Life Technologies目錄#PA519462,在PBS中1:50稀釋?zhuān)徊ㄐ蔚鞍讍慰寺】贵w(J144):Invitrogen目錄#MA3 - 745,在PBS中1:50稀釋?zhuān)T谟肨BS - Tween進(jìn)行三次額外洗滌步驟后,將150nL的二抗混合物(山羊抗兔IgG,DyLightTM594:ThermoScientific#UJ291725,1:250和山羊抗小鼠IgG(H&L),DyLightTM 488:ThermoScientific#UJ291725,1:250)和核標(biāo)記物Hoechst(Hoechst 33343:ThermoScientific,#62248)分配到每個(gè)斑點(diǎn)上,并在DMA上孵育1小時(shí)。在TBS中進(jìn)行三次洗滌后,用Mowiol將細(xì)胞包埋。使用Keyence BZ - 9000顯微鏡(Keyence,大阪,日本),用2X和10X物鏡拍攝明場(chǎng)和熒光顯微鏡圖像。
【參考文獻(xiàn)】
M. Benz, A. Asperger, M. Hamester, A. Welle, S. Heissler, & P.A. Levkin. A combined high-throughput and high-content platform for unified on-chip synthesis, characterization and biological screening, Nature Communications, 2020, 11 (5391).
E. Ueda, W. Feng, and P. A. Levkin. Superhydrophilic–superhydrophobic patterned surfaces as high-density cell microarrays: Optimization of reverse transfection, Healthcare Mater, 2016, 5 (2646).
A.A. Popova, D. Marcato, R. Peravali, I.A. Wehl, U. Schepers, & P.A. Levkin. Fish-microarray: miniaturized platform for single-embryo high-throughput screenings, Advanced Functional Materials, 2018, 28 (1703486).
W. Lei, K. Demir, J. Overhage, M. Grunze, T. Schwartz, & P.A. Levkin. Droplet-Microarray: Miniaturized platform for high-throughput screening of antimicrobial compounds, Advanced Biosystems, 2020, 4 (2000073).
A.A. Popova, S. Dietrich, W. Huber, M. Reischl, R. Peravali, & P.A. Levkin. Miniaturized drug sensitivity and resistance test on patient-derived cells using Droplet-Microarray, SLAS TECHNOLOGY Translating Life Sciences Innovation, 2021, 26 (274).

微信掃碼在線客服