AGENT BRAND
品牌專(zhuān)題當(dāng)前位置:首頁(yè) > 品牌專(zhuān)題
本篇主要介紹通過(guò)靶向脂肪性肝病 (SLD) 中的代謝因子來(lái)推進(jìn)代謝功能障礙相關(guān)脂肪性肝病 (MASLD) 和代謝功能障礙相關(guān)脂肪性肝炎 (MASH) 研究的系列文章。在本系列中,每篇文章都涵蓋了與脂肪性肝病代謝功能障礙相關(guān)的特定領(lǐng)域,為用于研究這些疾病中代謝功能障礙的策略和研究工具提供了指南。
全系列涵蓋:
推進(jìn)MASLD和MASH研究:簡(jiǎn)介
推進(jìn)MASLD和MASH研究:針對(duì)新發(fā)脂肪生成和胰島素抵抗
推進(jìn)MASLD和MASH研究:PPAR和FFAR脂肪酸信號(hào)通路
推進(jìn)MASLD和MASH研究:LXRs、FXRs和GP-BAR1在代謝調(diào)節(jié)中的作用
通過(guò)探索這些主題,發(fā)現(xiàn)支持您研究的產(chǎn)品和資源。
代謝功能障礙相關(guān)脂肪性肝病 (MASLD),以前稱(chēng)為非酒精性脂肪性肝病 (NAFLD),是一種復(fù)雜且異質(zhì)性的肝臟疾病。1MASLD 的特征是脂質(zhì)在肝細(xì)胞中異常積累,這種情況稱(chēng)為肝脂肪變性。1MASLD 可發(fā)展為更嚴(yán)重的形式,稱(chēng)為代謝功能障礙相關(guān)肝脂肪性肝炎 (MASH)。在這個(gè)階段,肝臟會(huì)經(jīng)歷持續(xù)的炎癥和細(xì)胞損傷。2如果沒(méi)有阻止或逆轉(zhuǎn) MASH 進(jìn)展的有效療法,MASH 患者有患肝硬化的風(fēng)險(xiǎn)。肝硬化是一種嚴(yán)重的進(jìn)行性疾病,其特征是廣泛的肝纖維化,可能導(dǎo)致肝功能喪失。


| MASLD | MASH |
| 代謝功能障礙相關(guān)的脂肪性肝 | 代謝功能障礙相關(guān)的脂肪性肝炎 |
| 一種輕度的 SLD,在沒(méi)有肝損傷或炎癥的情況下,肝臟中存在脂肪變性。6 | 一種更嚴(yán)重的 SLD 形式,其特征是在存在持續(xù)肝臟炎癥的情況下脂肪變性。7 |
| 通常為非進(jìn)展性且相對(duì)良性。6 | 可能會(huì)發(fā)展為更嚴(yán)重的疾病,如肝纖維化和肝硬化。8 |
區(qū)分 MASLD 和 MASH 很重要,因?yàn)樗鼈兙哂胁煌那熬昂拖嚓P(guān)風(fēng)險(xiǎn)。患有 MASH 的個(gè)體有患上更嚴(yán)重疾病的風(fēng)險(xiǎn),例如心血管疾病、癌癥、肝硬化和肝功能衰竭。9MASLD 和 MASH 都被認(rèn)為是可逆的,但當(dāng)疾病發(fā)展為肝硬化時(shí),移植可能是唯一的選擇。
|
|
|
全球 30% 的人口受到 MASLD 的影響10 | MASLD 相關(guān)死亡率正在增加10 | 只有一種 FDA 批準(zhǔn)的 MASH 療法11 |
MASLD 是世界上最常見(jiàn)的肝病,估計(jì)影響全球 30% 的人口,在某些地區(qū)區(qū)域患病率超過(guò) 40%。10,12MASLD 的患病率在全球范圍內(nèi)不斷增加,并且與肥胖和糖尿病發(fā)病率的上升相吻合。10因此,MASLD 與各種代謝危險(xiǎn)因素密切相關(guān),包括肥胖、血脂異常和胰島素抵抗/2 型糖尿病。13,14
直到最近,還沒(méi)有治療 MASLD 的藥物選擇,治療策略側(cè)重于生活方式的改變。2024 年 3 月,美國(guó) FDA 批準(zhǔn) resmetirom 用于治療 MASH。11
肝脂肪變性是 MASLD 和 MASH 等 SLD 的標(biāo)志(圖 1)。它的特征是脂質(zhì),尤其是甘油三酯 (TGs) 在肝細(xì)胞中以脂滴的形式在細(xì)胞內(nèi)積累。15這種積累是由過(guò)量的脂質(zhì)引起的,這是由于脂肪酸攝取、合成、輸出和氧化的不平衡造成的,并且是由許多潛在因素介導(dǎo)的。16
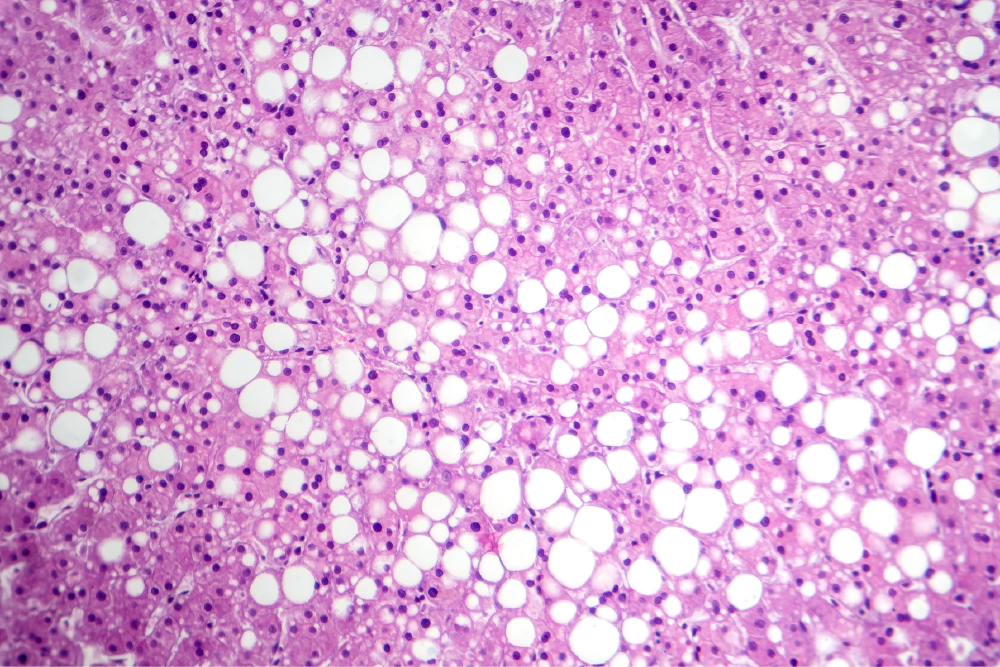
圖 1.肝脂肪變性的顯微照片顯示肝細(xì)胞中脂質(zhì)的積累。
MASLD 的發(fā)生和發(fā)展受多種因素的影響,包括遺傳和表觀遺傳、飲食和環(huán)境以及代謝因素,這些因素都導(dǎo)致了其復(fù)雜性。17顧名思義,MASLD 與肥胖、胰島素抵抗和糖尿病、血脂異常和代謝綜合征等疾病相關(guān)的代謝失調(diào)密切相關(guān)。解決潛在的代謝失調(diào)是 MASLD 治療的關(guān)鍵策略。
MASLD 是由于葡萄糖和脂質(zhì)代謝改變引起的能量穩(wěn)態(tài)失衡引起的。幾種失調(diào)導(dǎo)致肝臟中過(guò)量脂質(zhì)的積累,包括從頭脂肪生成、脂肪分解增加以及脂肪酸氧化和脂質(zhì)輸出減少(圖 2)。13,14,16這會(huì)導(dǎo)致肝臟脂質(zhì)積累,從而導(dǎo)致肝臟脂肪變性。
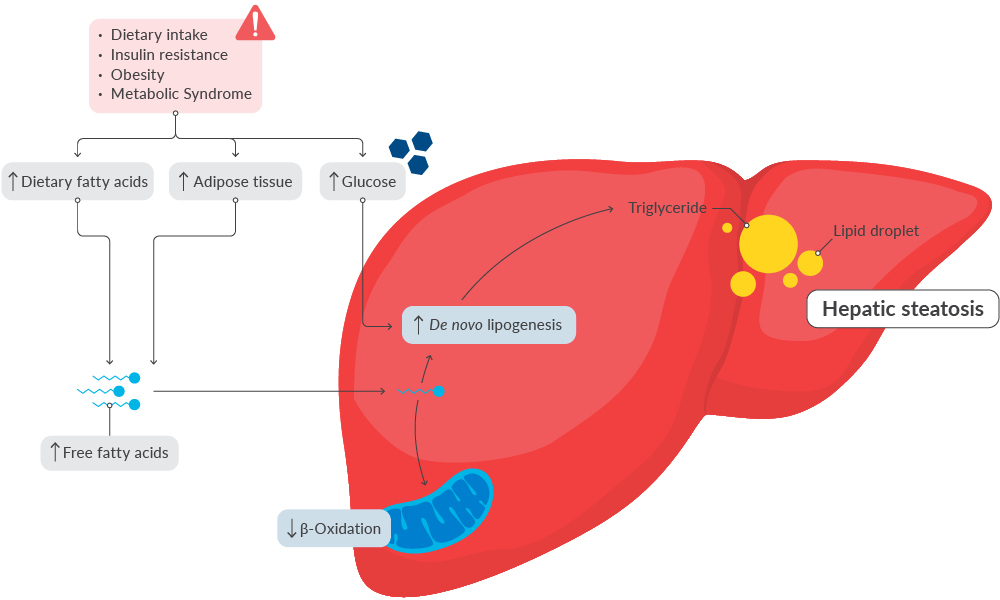
圖 2.導(dǎo)致 MASLD 中肝脂質(zhì)積累的途徑總結(jié)。圖修改自 Meex, R.C.R. 和 Watt, M.J. 肝因子:將非酒精性脂肪肝與胰島素抵抗聯(lián)系起來(lái)。 內(nèi)分泌 13(9),509-520 (2017)。18
肝脂肪變性及其相關(guān)的代謝紊亂可在肝臟中產(chǎn)生級(jí)聯(lián)效應(yīng)。它損害調(diào)節(jié)新陳代謝和細(xì)胞功能的細(xì)胞信號(hào)級(jí)聯(lián)反應(yīng),并誘導(dǎo)炎癥和細(xì)胞損傷,共同促進(jìn)肝損傷和疾病進(jìn)展。19
針對(duì) MASLD 代謝紊亂的治療策略旨在減少代謝損傷和壓力。通過(guò)靶向這些代謝過(guò)程,可以減少隨后的肝脂肪變性、炎癥和它們引起的細(xì)胞損傷,從而有可能阻止這種情況的進(jìn)展。20
通過(guò)量化脂肪變性或測(cè)量廣泛使用的肝損傷標(biāo)志物的水平來(lái)測(cè)量肝損傷程度的檢測(cè)對(duì)于 MASLD 研究至關(guān)重要。
| 產(chǎn)品貨號(hào) | 產(chǎn)品名稱(chēng) | 描述 |
| 10012643 | 脂肪變性比色測(cè)定試劑盒 | 檢測(cè)細(xì)胞中脂質(zhì)的過(guò)度積累。 |
| 700260 | 丙氨酸轉(zhuǎn)氨酶比色活性測(cè)定試劑盒 | 測(cè)量血清、血漿、組織樣品和細(xì)胞裂解物中的 ALT 活性。 |
| 701710 | 堿性磷酸酶比色活性測(cè)定試劑盒 | 一種比色測(cè)定法,用于檢測(cè)血漿、血清、組織樣品和細(xì)胞裂解物中 ALP 活性。 |
| 701640 | 天冬氨酸轉(zhuǎn)氨酶比色活性測(cè)定試劑盒 | 測(cè)量血清、血漿、組織樣品和細(xì)胞裂解物中的 AST 活性。 |
| 501760 | 白蛋白(人)ELISA 試劑盒 | 用于白蛋白定量的競(jìng)爭(zhēng)性 ELISA。 |
總之,MASLD 是代謝因子復(fù)雜相互作用的結(jié)果,最終導(dǎo)致肝脂肪變性并可能發(fā)展為更嚴(yán)重的脂肪性肝病。隨著研究的繼續(xù),MASLD 的發(fā)病機(jī)制涉及幾種關(guān)鍵的代謝失調(diào),包括新發(fā)脂肪生成、胰島素抵抗和脂質(zhì)穩(wěn)態(tài)。
引用:
1. Syed-Abdul, M.M. Lipid metabolism in metabolic-associated steatotic liver disease (MASLD). Metabolites 14(1), 12 (2024).
2. Chan, W.-K., Chuah, K.-H., Rajaram, R.B., et al. Metabolic dysfunction-associated steatotic liver disease (MASLD): A state-of-the-art review. J. Obes. Metab. Syndr. 32(3), 197-213 (2023).
3. Acharya, P., Chouhan, K., Weiskirchen, S. et al. Cellular mechanisms of liver fibrosis. Front. Pharmacol. 12, 671640 (2021).
4. Rinella, M.E., Lazarus, J.V., Ratziu, V., et al. A multisociety Delphi consensus statement on new fatty liver disease nomenclature. Hepatology 78(6), 1966-1986 (2023).
5. Eslam, M., Sanyal, A.J., George, J., et al. MAFLD: A consensus-driven proposed nomenclature for metabolic associated fatty liver disease. Gastroentero?logy 158?(7), 1999-2014.e1 (2020).
6. Armandi, A. and Bugianesi, E. Dietary and pharmacological treatment in patients with metabolic-dysfunction associated steatotic liver disease. Eur. J. Intern. Med. 122, 20-27 (2024).
7. Ghazanfar, H., Javed, N., Qasim, A., et al. Metabolic dysfunction-associated steatohepatitis and progression to hepatocellular carcinoma: A literature review. Cancers (Basel) 16(6), 1214 (2024).
8. Paklar, N., Mijic, M., and Filipec-Kanizaj, T. The outcomes of liver transplantation in severe metabolic dysfunction-associated steatotic liver disease patients. Biomedicines 11(11), 3096 (2023).
9. Westfall, E.C., Jeske, R., and Bader, A.R. Nonalcoholic fatty liver disease: Common questions and answers on diagnosis and management. Am. Fam. Physician 102(10), 603-612 (2020).
10. Teng, M.L., Ng., C.H., Huang, D.Q., et al. Global incidence and prevalence of nonalcoholic fatty liver disease. Clin. Mol. Hepatol. 29(Suppl), S32-S42 (2023).
11. Petta, S., Targher, G., Romeo, S., et al. The first MASH drug therapy on the horizon: Current perspectives of resmetirom. Liver Int. 44(7), 1526-1536 (2024).
12. Cotter, T.G. and Rinella, M. Nonalcoholic fatty liver disease 2020: The state of the disease. Gastroenterology 158(7), 1851-1864 (2020).
13. Schuppan, D. and Schattenberg, J.M. Non-alcoholic steatohepatitis: Pathogenesis and novel therapeutic approaches. J. Gastroenterol. Hepatol. 28(Suppl1), 68-76 (2013).
14. Godoy-Matos, A.F., Silva Júnior, W.S., and Valerio, C.M. NAFLD as a continuum: From obesity to metabolic syndrome and diabetes. Diabetol. Metab. Syndr. 12, 60 (2020).
15. Alamri, H., Patterson, N.H., Yang, E., et al. Mapping the triglyceride distribution in NAFLD human liver by MALDI imaging mass spectrometry reveals molecular differences in micro and macro steatosis. Anal. Bioanal. Chem. 411(4), 885-894 (2019).
16. Chiappini, F., Coilly, A., Kadar, H., et al. Metabolism dysregulation induces a specific lipid signature of nonalcoholic steatohepatitis in patients. Sci. Rep.7, 46658 (2017).
17. Buzzetti, E., Pinzani, M., and Tsochatzis, E.A. The multiple-hit pathogenesis of non-alcoholic fatty liver disease (NAFLD). Metabolism 65(8), 1038-1048 (2016).
18. Meex, R.C.R. and Watt, M.J. Hepatokines: Linking nonalcoholic fatty liver disease and insulin resistance. Nat. Rev. Endocrinol. 13(9), 509-520 (2017).
19. Chakravarthy, M.V. and Neuschwander-Tetri, B.A. The metabolic basis of nonalcoholic steatohepatitis. Endocrinol. Diabetes Metab. 3(4), e00112 (2020).
20. Tacke, F., Puengel, T., Loomba, R., et al. An integrated view of anti-inflammatory and antifibrotic targets for the treatment of NASH. J. Hepatol. 79(2), 552-566 (2023).

微信掃碼在線客服