PRODUCT CENTER
特色產(chǎn)品當前位置:首頁 > 特色產(chǎn)品
這篇發(fā)表于《Nature Communications》的研究論文《Elevated extracellular matrix protein 1 in circulating extracellular vesicles supports breast cancer progression under obesity conditions》(肥胖條件下細胞外基質蛋白循環(huán)細胞外囊泡促進乳腺癌進展)系統(tǒng)性地探討了肥胖條件下循環(huán)小細胞外囊泡(sEVs)中細胞外基質蛋白1(ECM1)的表達升高及其在促進乳腺癌(BC)進展中的作用機制。

研究背景
肥胖是乳腺癌(BC)的重要風險因素,與腫瘤體積增大、轉移率升高及不良預后顯著相關。既往研究聚焦于脂肪細胞功能障礙(如脂聯(lián)素、瘦素分泌異常),但循環(huán)小細胞外囊泡(sEVs)在肥胖相關乳腺癌中的作用機制尚未明確。sEVs是直徑50-200 nm的脂質雙層囊泡,可攜帶蛋白質、核酸等生物活性分子,介導細胞間通訊并影響腫瘤微環(huán)境。
本研究首次揭示:肥胖通過整合素β2依賴性途徑增加循環(huán)sEVs中ECM1(細胞外基質蛋白1)的裝載,進而促進乳腺癌轉移與生長。
關鍵實驗與SBI Exo-Fect Kit的應用
實驗目的:為了明確sEVs中ECM1蛋白的功能性作用,研究人員需要將外源性ECM1基因構建體高效導入sEVs中,構建“ECM1過表達sEVs”(簡稱ECM-sEVs),用于后續(xù)功能驗證和體內(nèi)治療實驗。
在驗證ECM1促癌功能的關鍵實驗中,研究團隊使用SBI Exo-Fect Exosome Transfection Kit(貨號EXFT10A-1)進行sEVs的工程化改造。
技術優(yōu)勢與價值:
高效裝載:通過脂質體介導的膜融合,將外源ECM1基因直接導入天然sEVs,避免細胞轉染的脫靶效應。
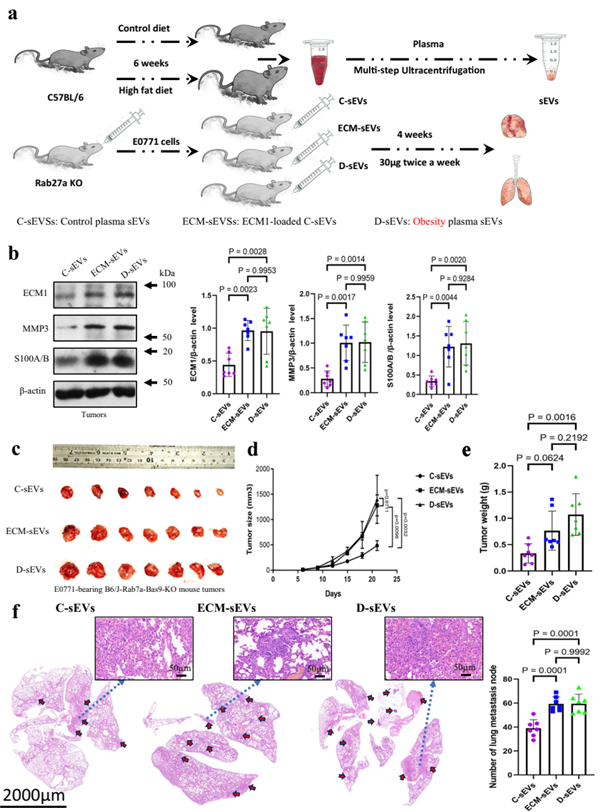
功能驗證:ECM-sEVs注射至Rab27a敲除小鼠(sEVs分泌缺陷)后,成功恢復腫瘤ECM1/MMP3/S100A/B表達水平,證實sEVs遞送的ECM1直接驅動乳腺癌進展(圖6b-f)。
轉化意義:首次實現(xiàn)肥胖相關sEVs致癌分子的功能重建,為sEVs靶向治療提供技術基礎。
主要研究結論
1. 肥胖上調循環(huán)sEVs中ECM1表達:在人和小鼠模型中均得到驗證。
2. 整合素-β2介導ECM1裝載入sEVs:在巨噬細胞和脂肪細胞中,integrin-β2表達升高,促進ECM1進入sEVs,而不影響細胞內(nèi)ECM1水平。
3. sEVs傳遞ECM1至乳腺癌細胞:肥胖來源的sEVs(D-sEVs/H-sEVs)能有效將ECM1蛋白遞送至癌細胞,提升其侵襲與遷移能力。
4. ECM1促進MMP3和S100A/B表達:進而增強腫瘤惡性表型。
5. Rab27a敲除抑制肥胖促癌效應:sEVs分泌缺陷小鼠中,肥胖未能增強腫瘤生長與轉移。
6. 工程化sEVs模擬病理功能:通過Exo-Fect成功構建ECM1過表達sEVs,證實其具有促瘤功能。
研究結論
機制創(chuàng)新:肥胖通過整合素β2增加ECM1在循環(huán)sEVs中的裝載,sEVs遞送ECM1至乳腺癌細胞后激活MMP3/S100A/B通路,促進轉移與生長。
轉化價值:循環(huán)sEVs的ECM1可作為肥胖相關乳腺癌的診斷標志物。
SBI Exo-Fect試劑盒成功實現(xiàn)sEVs的工程化改造,為基于sEVs的靶向遞送系統(tǒng)(如裝載ECM1抑制劑)提供技術支撐。
該研究不僅深化了對肥胖相關乳腺癌機制的理解,也為開發(fā)基于sEVs的診斷標志物和治療策略提供了新思路。未來,利用類似Exo-Fect的sEVs工程化技術,有望實現(xiàn)針對肥胖相關乳腺癌的精準干預和治療。

微信掃碼在線客服