TECHNICAL COLUMN
學(xué)習(xí)資源當(dāng)前位置:首頁 > 學(xué)習(xí)資源
2023年9月12日,來自中國科學(xué)院大學(xué)存濟(jì)醫(yī)學(xué)院施一等研究人員合作在《自然》雜志發(fā)表了標(biāo)題為“Molecular mechanism of de novo replication by the Ebola virus polymerase”的研究成果,揭示埃博拉病毒聚合酶從頭復(fù)制的分子機(jī)制。
埃博拉出血熱(EBHF)被認(rèn)為是當(dāng)今世界上非常致命的病毒性出血熱之一,感染者的死亡率在50%至90%之間。感染者經(jīng)歷了一系列可怕的病程,病毒在體內(nèi)迅速擴(kuò)散并大量繁殖,嚴(yán)重?fù)p害多個(gè)器官,導(dǎo)致其變形、壞死,并逐漸分解。病人不可避免地走向死亡。
據(jù)介紹,nsNSV,包括EBOV、狂犬病病毒、人類呼吸道合胞病毒和肺炎病毒,可導(dǎo)致人類和動(dòng)物呼吸道感染、出血熱和腦炎,被認(rèn)為是全球重大的健康和經(jīng)濟(jì)負(fù)擔(dān)。病毒基因組的復(fù)制和轉(zhuǎn)錄是由大型L聚合酶完成的,該聚合酶是開發(fā)抗病毒藥物的一個(gè)很有前景的靶點(diǎn)。
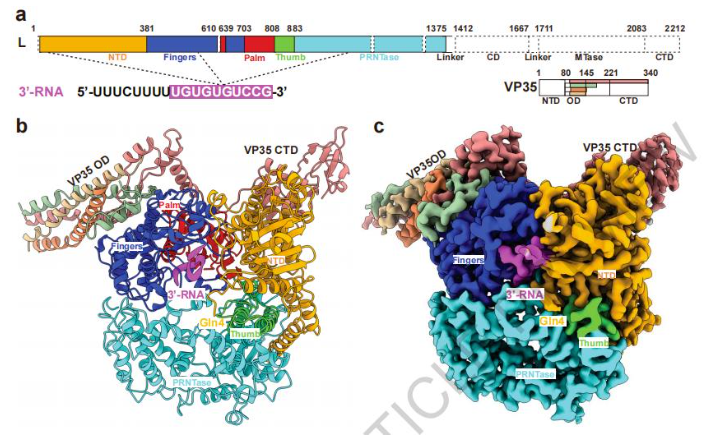
埃博拉病毒聚合酶L-VP35-RNA復(fù)合物的整體結(jié)構(gòu)
研究人員以埃博拉病毒(EBOV)L聚合酶為代表,通過酶切實(shí)驗(yàn)表明,L聚合酶的從頭復(fù)制受EBOV基因組特定3'前導(dǎo)序列的控制,至少三個(gè)堿基對(duì)的形成可有效驅(qū)動(dòng)RNA合成的延伸過程,而不受特定RNA序列的影響。研究人員隨后測(cè)定了EBOV L-VP35-RNA復(fù)合物的高分辨率結(jié)構(gòu),發(fā)現(xiàn)3'前導(dǎo)RNA以獨(dú)特的穩(wěn)定彎曲構(gòu)象結(jié)合在模板入口通道中。
進(jìn)一步的誘變工作證實(shí)了RNA的彎曲構(gòu)象是從頭復(fù)制活性所需的,并揭示了L蛋白中穩(wěn)定RNA構(gòu)象的關(guān)鍵殘基。這些發(fā)現(xiàn)為非節(jié)段負(fù)鏈RNA病毒(nsNSV)聚合酶的RNA合成提供了新的機(jī)理認(rèn)識(shí),并揭示了開發(fā)抗病毒藥物的重要靶點(diǎn)。
文章來源:
Peng, Qi, Yuan, Bin, Cheng et al, Molecular mechanism of de novo replication by the Ebola virus polymerase.DOI: 10.1038/s41586-023-06608-1 最新IF:69.504

微信掃碼在線客服