TECHNICAL COLUMN
學(xué)習(xí)資源當(dāng)前位置:首頁 > 學(xué)習(xí)資源
2023年7月3日,美國紀(jì)念斯隆凱特琳癌癥中心(Memorial Sloan Kettering Cancer Center, MSKCC)Kristian Helin研究組在Molecular Cell發(fā)表文章Chromatin regulation of transcriptional enhancers and cell fate by the Sotos syndrome gene NSD1,揭示了NSD1不依賴酶活性促進(jìn)基因轉(zhuǎn)錄的功能并且闡釋了NSD1對細(xì)胞分化的影響,增進(jìn)了對NSD1參與Sotos綜合征病理機(jī)制的理解。

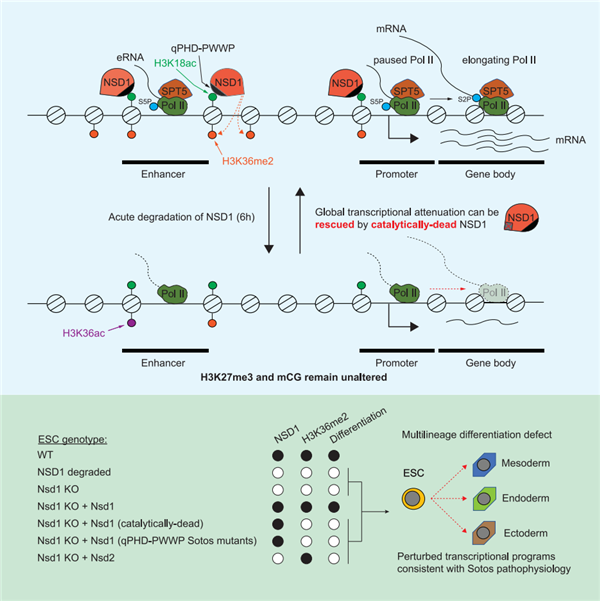
作者們以小鼠胚胎干細(xì)胞(ESC)為模型,首先通過基因敲除和靶向蛋白降解(dTAG)的方法,發(fā)現(xiàn)Nsd1敲除或降解可以消除細(xì)胞內(nèi)幾乎全部的H3K36me2,證明了NSD1為胚胎干細(xì)胞中的決定性H3K36me2催化酶。NSD1的基因組分布仍然未知,作者們通過CUT&RUN技術(shù)發(fā)現(xiàn)NSD1和H3K36me2富集于活躍增強(qiáng)子區(qū)域,并且在胚胎干細(xì)胞向上胚層干細(xì)胞(EpiSC)分化過程中它們的分布變化與增強(qiáng)子活性變化緊密相關(guān)。NSD1有多個(gè)與染色質(zhì)結(jié)合相關(guān)的結(jié)構(gòu)域,然而它們的功能仍不清楚。作者們通過在NSD1敲除的胚胎干細(xì)胞表達(dá)一些列NSD1突變體,發(fā)現(xiàn)一個(gè)由四聯(lián)PHD(PHD1-4)和臨近PWWP2結(jié)構(gòu)域構(gòu)成的功能區(qū)域(qPHD-PWWP module)對NSD1的染色質(zhì)結(jié)合及增強(qiáng)子富集有關(guān)鍵作用。作者們進(jìn)一步通過生化互作實(shí)驗(yàn)發(fā)現(xiàn)該功能區(qū)域可結(jié)合H3K18ac修飾的核小體。細(xì)胞內(nèi)的H3K18ac由富集于增強(qiáng)子的乙酰化酶p300/CBP催化且與NSD1同樣富集于活躍增強(qiáng)子區(qū)域。值得注意的是,Sotos綜合征相關(guān)的NSD1錯(cuò)意突變在該qPHD-PWWP區(qū)域集中分布,并且作者們發(fā)現(xiàn)位于qPHD-PWWP區(qū)域的Sotos突變會引起NSD1染色質(zhì)和增強(qiáng)子的結(jié)合障礙以及細(xì)胞內(nèi)H3K36me2的缺失。
為了進(jìn)一步研究NSD1和H3K36me2缺失對組蛋白和DNA修飾的影響,作者們通過基因組編輯在內(nèi)源Nsd1位點(diǎn)插入蛋白降解序列(dTAG)以實(shí)現(xiàn)快速NSD1誘導(dǎo)降解 – 誘導(dǎo)分子dTAG-13處理1小時(shí)即可引起近乎完全的NSD1降解。H3K36me2在處理6小時(shí)后有顯著下降(大于50%)并于18-24小時(shí)近乎完全消失。值得注意的是,NSD1降解在至少24小時(shí)內(nèi)(24-72小時(shí))不影響H3K27me3和DNA甲基化,雖然作者們與之前報(bào)道同樣發(fā)現(xiàn)NSD1/H3K36me2長時(shí)間缺失缺失(如在基因敲除或長時(shí)間dTAG-13處理的情況下)可引起H3K27me3的增加和DNA甲基化的減少。利用該具有高時(shí)間分辨率的系統(tǒng),作者們進(jìn)一步研究了NSD1降解在短時(shí)程內(nèi)對基因轉(zhuǎn)錄的直接影響。通過SLAM-seq新生RNA分析技術(shù),作者們發(fā)現(xiàn)NSD1降解6小時(shí)以內(nèi)即會引起廣泛的基因轉(zhuǎn)錄下調(diào),而幾乎沒有基因表達(dá)上調(diào)。值得注意的是,轉(zhuǎn)基因表達(dá)的缺失H3K36me2催化活性的NSD1突變體與野生型NSD1同樣可以挽救內(nèi)源NSD1降解引發(fā)的基因轉(zhuǎn)錄下調(diào),說明NSD1存在不依賴酶活性的轉(zhuǎn)錄促進(jìn)功能。與其形成鮮明對比的是,利用同樣系統(tǒng)誘導(dǎo)SETD2(H3K36me3催化酶)降解只能引發(fā)少量基因的差異表達(dá)(上調(diào)或下調(diào))。作者們近一步發(fā)現(xiàn),NSD1降解(6小時(shí))引發(fā)增強(qiáng)子活性下降和RNA聚合酶由啟動子附近暫停區(qū)域向轉(zhuǎn)錄延伸區(qū)域的釋放發(fā)生障礙,并且發(fā)現(xiàn)延伸因子SPT5(DSIF復(fù)合體亞基)在增強(qiáng)子和基因區(qū)域的結(jié)合顯著下調(diào)。
最后,作者們研究了NSD1缺失或突變對胚胎干細(xì)胞分化過程中基因表達(dá)的影響。利用類胚體(embryoid body)分化,作者們發(fā)現(xiàn)NSD1降解導(dǎo)致內(nèi)、中、外三個(gè)胚層分化相關(guān)基因表達(dá)下調(diào)和相關(guān)增強(qiáng)子激活障礙,并且受影響基因相關(guān)的生物學(xué)過程與Sotos綜合征的病理特征相符。由于Sotos綜合征患者表現(xiàn)智力發(fā)育障礙,作者們利用定向前腦類器官分化技術(shù)發(fā)現(xiàn)NSD1降解引發(fā)神經(jīng)分化障礙。作者們進(jìn)一步發(fā)現(xiàn)qPHD-PWWP區(qū)域缺失或位于該區(qū)域的Sotos相關(guān)突變也會引發(fā)顯著分化基因激活障礙。
該工作發(fā)現(xiàn)NSD1為一個(gè)新的轉(zhuǎn)錄增強(qiáng)子調(diào)控蛋白,并揭示了其調(diào)控基因表達(dá)和細(xì)胞分化的機(jī)制。值得注意的是,該工作揭示了NSD1與MLL3/4(H3K4me1催化酶)功能上的相似性:1)均催化低程度甲基化(一或二甲基化);2)均調(diào)控增強(qiáng)子功能且可通過不依賴酶活性方式調(diào)節(jié)基因轉(zhuǎn)錄;3)均影響RNA聚合酶從啟動子暫停狀態(tài)釋放進(jìn)入轉(zhuǎn)錄延伸的過程;4)均為胚胎干細(xì)胞分化必須的因子【10-12】。該工作的發(fā)現(xiàn)也提示組蛋白修飾酶可能廣泛存在非酶促活性依賴的基因轉(zhuǎn)錄調(diào)節(jié)功能,從而需要在將來的研究中仔細(xì)發(fā)掘該類功能并闡釋它們的具體機(jī)制。最后,該工作也提示可利用基因編輯和干細(xì)胞分化技術(shù)體外模擬Sotos綜合征并研究其病理機(jī)制。
美國紀(jì)念斯隆凱特琳癌癥中心的孫稹博士(目前為Charles Sawyers實(shí)驗(yàn)室博士后研究員)為本文的獨(dú)立第一作者和共同通訊作者,Kristian Helin教授(現(xiàn)為英國癌癥研究院(Institute of Cancer Research, ICR)首席執(zhí)行官兼主席)為共同通訊作者。該工作也得到了紀(jì)念斯隆凱特琳癌癥中心Charles Sawyers教授(人類腫瘤及病理學(xué)系(HOPP)主任及霍華德休斯研究員)及合作者們的大力支持。孫稹博士的工作受到Edith C. Blum Foundation和MSKCC Functional Genomics Initiative的支持。孫稹博士在2023年6月的國際干細(xì)胞研究學(xué)會年會(ISSCR 2023)上首次正式報(bào)道這一工作。
孫稹博士于西奈山醫(yī)學(xué)院(Icahn School of Medicine at Mount Sinai)獲得博士學(xué)位,師從Emily Bernstein教授從事組蛋白變體的研究(Sun et al. Nat Struct Mol Biol, 2018【13】)。他于2019年加入紀(jì)念斯隆凱特琳癌癥中心Kristian Helin實(shí)驗(yàn)室開始博士后研究,并于2021年(Kristian Helin教授遷至英國)加入同一中心的Charles Sawyers實(shí)驗(yàn)室,目前從事染色質(zhì)和轉(zhuǎn)錄調(diào)控在前列腺癌中的功能研究。
原文鏈接:
https://doi.org/10.1016/j.molcel.2023.06.007
文獻(xiàn)參考:
1. Wagner, E.J., and Carpenter, P.B. (2012). Understanding the language of Lys36 methylation at histone H3. Nat. Rev. Mol. Cell Biol. 13, 115–126. 10.1038/nrm3274.
2. Schmitges, F.W., Prusty, A.B., Faty, M., Stützer, A., Lingaraju, G.M., Aiwazian, J., Sack, R., Hess, D., Li, L., Zhou, S., et al. (2011). Histone Methylation by PRC2 Is Inhibited by Active Chromatin Marks. Mol. Cell 42, 330–341. 10.1016/j.molcel.2011.03.025.
3. Yuan, W., Xu, M., Huang, C., Liu, N., Chen, S., and Zhu, B. (2011). H3K36 methylation antagonizes PRC2-mediated H3K27 methylation. J. Biol. Chem. 286, 7983–7989. 10.1074/jbc.M110.194027.
4. Weinberg, D.N., Papillon-Cavanagh, S., Chen, H., Yue, Y., Chen, X., Rajagopalan, K.N., Horth, C., McGuire, J.T., Xu, X., Nikbakht, H., et al. (2019). The histone mark H3K36me2 recruits DNMT3A and shapes the intergenic DNA methylation landscape. Nature 573, 281–286. 10.1038/s41586-019-1534-3.
5. Chen, H., Hu, B., Horth, C., Bareke, E., Rosenbaum, P., Kwon, S.Y., Sirois, J., Weinberg, D.N., Robison, F.M., Garcia, B.A., et al. (2022). H3K36 dimethylation shapes the epigenetic interaction landscape by directing repressive chromatin modifications in embryonic stem cells. Genome Res. 32, 825–837. 10.1101/gr.276383.121.
6. Streubel, G., Watson, A., Jammula, S.G., Scelfo, A., Fitzpatrick, D.J., Oliviero, G., McCole, R., Conway, E., Glancy, E., Negri, G.L., et al. (2018). The H3K36me2 Methyltransferase Nsd1 Demarcates PRC2-Mediated H3K27me2 and H3K27me3 Domains in Embryonic Stem Cells. Mol. Cell 70, 371-379.e5. 10.1016/j.molcel.2018.02.027.
7. Jani, K.S., Jain, S.U., Ge, E.J., Diehl, K.L., Lundgren, S.M., Müller, M.M., Lewis, P.W., and Muir, T.W. (2019). Histone H3 tail binds a unique sensing pocket in EZH2 to activate the PRC2 methyltransferase. Proc. Natl. Acad. Sci. U. S. A. 116, 8295–8300. 10.1073/pnas.1819029116.
8. Finogenova, K., Bonnet, J., Poepsel, S., Sch?fer, I.B., Finkl, K., Schmid, K., Litz, C., Strauss, M., Benda, C., and Müller, J. (2020). Structural basis for PRC2 decoding of active histone methylation marks H3K36me2/3. Elife 9, 1–30. 10.7554/eLife.61964.
9. Huang, N., Vom Baur, E., Garnier, J.M., Lerouge, T., Vonesch, J.L., Lutz, Y., Chambon, P., and Losson, R. (1998). Two distinct nuclear receptor interaction domains in NSD1, a novel SET protein that exhibits characteristics of both corepressors and coactivators. EMBO J. 17, 3398–3412. 10.1093/emboj/17.12.3398.
10. Rickels, R., Herz, H.M., Sze, C.C., Cao, K., Morgan, M.A., Collings, C.K., Gause, M., Takahashi, Y.H., Wang, L., Rendleman, E.J., et al. (2017). Histone H3K4 monomethylation catalyzed by Trr and mammalian COMPASS-like proteins at enhancers is dispensable for development and viability. Nat. Genet. 49, 1647–1653. 10.1038/ng.3965.
11. Dorighi, K.M., Swigut, T., Henriques, T., Bhanu, N. V., Scruggs, B.S., Nady, N., Still, C.D., Garcia, B.A., Adelman, K., and Wysocka, J. (2017). Mll3 and Mll4 Facilitate Enhancer RNA Synthesis and Transcription from Promoters Independently of H3K4 Monomethylation. Mol. Cell 66, 568-576.e4. 10.1016/j.molcel.2017.04.018.
12. Xie, G., Lee, J.-E., Senft, A.D., Park, Y.-K., Jang, Y., Chakraborty, S., Thompson, J.J., McKernan, K., Liu, C., Macfarlan, T.S., et al. (2023). MLL3/MLL4 methyltransferase activities control early embryonic development and embryonic stem cell differentiation in a lineage-selective manner. Nat. Genet., 2020.09.14.296558. 10.1038/s41588-023-01356-4.
13. Sun, Z., Filipescu, D., Andrade, J., Gaspar-Maia, A., Ueberheide, B., and Bernstein, E. (2018). Transcription-associated histone pruning demarcates macroH2A chromatin domains. Nat. Struct. Mol. Biol. 25, 958–970. 10.1038/s41594-018-0134-5.

微信掃碼在線客服