PRODUCT CENTER
特色產(chǎn)品當前位置:首頁 > 特色產(chǎn)品
在腫瘤治療領(lǐng)域,PARP抑制劑已取得顯著成功,其作用機制不僅在于抑制PARP酶的催化活性,更關(guān)鍵的是將PARP蛋白“捕獲”在DNA損傷位點,形成致命的PARP-DNA復合物,導致癌細胞死亡。然而,第一代PARP抑制劑主要靶向PARP1,對PARP2的選擇性及捕獲效應研究相對不足。隨著研究發(fā)現(xiàn)PARP2在前列腺癌等惡性腫瘤中過表達,并通過FOXA1/AR通路參與疾病進展,開發(fā)能夠特異性誘導PARP2-DNA捕獲的小分子抑制劑成為新的藥物發(fā)現(xiàn)方向。
由艾美捷代理的BPS Bioscience推出的PARPtrap Assay Kit for PARP2(貨號:78296),正是為高通量篩選和表征PARP2捕獲型抑制劑而設計的完整解決方案。該試劑盒采用熒光偏振(Fluorescence Polarization, FP)技術(shù),在均相體系中實時檢測PARP2與DNA的結(jié)合狀態(tài),可快速評估化合物促進PARP2-DNA復合物形成的能力。以下從檢測原理、試劑盒組分、應用場景及操作要點等方面進行詳細介紹。
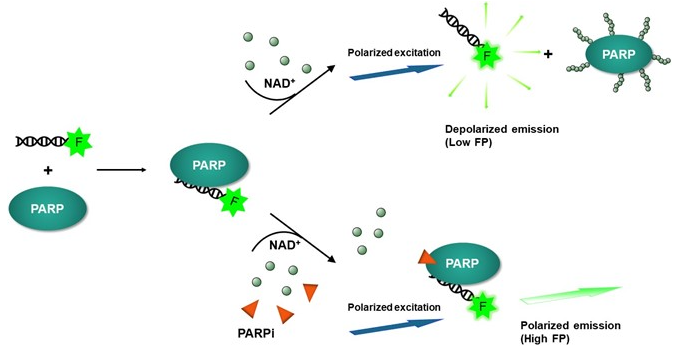
圖1:測定原理。
SARM1的水解酶活性是通過監(jiān)測Etheno-NAD水解形成Etheno-ADPR+煙酰胺的過程來測量的。由于內(nèi)部猝滅作用,Etheno-NAD本身不具有熒光性。當被SARM1水解時,煙酰胺被釋放出來,導致熒光信號增強,且熒光信號的增強與酶活性直接成正比。
一、檢測原理:熒光偏振法監(jiān)測PARP2-DNA相互作用
熒光偏振技術(shù)基于小分子在溶液中的旋轉(zhuǎn)速度與其分子量之間的關(guān)系。當熒光標記的小分子(如寡核苷酸探針)處于自由狀態(tài)時,旋轉(zhuǎn)速度快,發(fā)射光偏振程度低;當該分子與較大的蛋白質(zhì)(如PARP2)結(jié)合后,復合物旋轉(zhuǎn)速度減慢,發(fā)射光偏振程度顯著升高。
本試劑盒的核心設計如下:
1. 熒光標記的DNA雙鏈探針:提供一條末端帶有熒光基團(如FAM)的雙鏈寡核苷酸,模擬DNA損傷位點的結(jié)構(gòu)。
2. 重組人源PARP2酶(氨基酸2-583):包含完整的DNA結(jié)合域及催化域,具有NAD?依賴性自身核糖基化活性。
3. NAD?:作為PARP2的底物,在未添加抑制劑時,PARP2結(jié)合DNA后會發(fā)生自身PARylation,負電荷積累導致其從DNA上解離。
4. 待測化合物:若化合物具有“捕獲”功能,則會阻止PARP2從DNA上解離,使其穩(wěn)定結(jié)合在DNA探針上。
檢測流程:將PARP2酶、熒光DNA探針、NAD?及待測化合物混合孵育。在無捕獲劑時,PARP2結(jié)合DNA后迅速發(fā)生自身修飾并解離,熒光偏振值較低;在存在捕獲型抑制劑時,PARP2被鎖定在DNA上,形成高分子量復合物,熒光偏振值顯著升高。通過測定偏振值(mP)的變化,即可量化化合物的捕獲活性。
二、試劑盒組分與規(guī)格
該試劑盒提供兩種規(guī)格:96孔板形式(100次反應)和384孔板形式(400次反應),每個試劑盒包含:
重組人PARP2酶(2-583氨基酸,純度及活性經(jīng)質(zhì)控驗證)
熒光標記的寡核苷酸雙鏈(避光保存)
NAD?(需按說明溶解使用)
PARPtrap 檢測緩沖液(優(yōu)化了離子強度及pH,確保最佳結(jié)合效率)
詳細操作說明書
所有組分在收貨后按指示存儲(通常為-80°C),自收貨之日起6個月內(nèi)保持最佳性能。熒光探針對光敏感,建議分裝后避光保存,避免反復凍融。
三、核心應用場景
本試劑盒主要面向兩大藥物發(fā)現(xiàn)需求:
1. 高通量篩選(HTS)促進PARP2-DNA捕獲的小分子
傳統(tǒng)的PARP酶活性抑制試驗僅能反映化合物對催化活性的抑制,無法區(qū)分“催化抑制”與“DNA捕獲”兩種機制。而PARPtrap試劑盒直接檢測PARP2-DNA復合物的穩(wěn)定性,可精準識別能夠增強而非破壞該復合物的化合物。這對于開發(fā)具有更強細胞毒性效應的下一代PARP抑制劑(如PARP2選擇性捕獲劑)至關(guān)重要。試劑盒兼容自動化移液工作站,384孔板格式支持每天數(shù)千個化合物的篩選。
2. 先導化合物的IC??測定及機制表征
對于篩選出的陽性化合物,可進一步進行劑量-響應曲線分析,計算其促進PARP2-DNA捕獲的半效濃度(EC??)或IC??。由于熒光偏振讀數(shù)穩(wěn)定、Z'因子高,該方法能夠可靠區(qū)分不同化合物之間的效力差異。研究者還可以通過改變NAD?濃度或DNA序列,探究化合物的作用模式(如是否與DNA結(jié)合位點競爭)。
四、實驗流程簡要說明
1. 試劑準備:將PARP2酶、熒光DNA探針、NAD?及檢測緩沖液置于冰上解凍,避光保存熒光探針。準備待測化合物(建議使用DMSO溶解,并設置濃度梯度)。
2. 反應體系構(gòu)建(384孔板推薦方案):每孔加入10 uL檢測緩沖液,隨后加入2 uL PARP2酶(終濃度優(yōu)化范圍為10–100 nM),2 uL熒光DNA探針(終濃度5–20 nM),2 uL NAD?(終濃度100 uM),以及2 uL待測化合物或DMSO對照。總體積調(diào)整至20 uL。
3. 孵育與讀數(shù):室溫避光孵育30–60分鐘。使用熒光偏振酶標儀,激發(fā)波長485 nm,發(fā)射波長535 nm,分別測量平行偏振(S)和垂直偏振(P)信號,計算偏振值mP = 1000 × (S - G×P)/(S + G×P),其中G為儀器校正因子。
4. 數(shù)據(jù)分析:將化合物孔的mP值與陰性對照(無化合物,PARP2正常解離)及陽性對照(使用已知捕獲型抑制劑,如奧拉帕尼或特定PARP2工具化合物)進行比較。捕獲活性% = (mP_compound - mP_min) / (mP_max - mP_min) × 100%,繪制劑量-響應曲線擬合EC50。
五、注意事項與配套建議
物種特異性:試劑盒提供人源PARP2重組蛋白,其DNA結(jié)合域與嚙齒類動物同源性較高,但跨物種驗證需用戶自行評估。
陽性對照:首次使用建議運行已知的PARP捕獲劑(如talazoparib,雖主要靶向PARP1但對PARP2也有一定捕獲效應),以確認體系性能。
背景控制:無PARP2酶的孔作為空白對照,測定熒光探針的基礎(chǔ)偏振值。NAD?缺失的孔可反映最大結(jié)合信號(因無自身修飾解離)。
輔助設備:需要具備熒光偏振檢測模塊的多模式酶標儀,以及黑色、低自發(fā)熒光的384孔板。
干擾排除:某些化合物自身可能具有熒光或淬滅效應,建議設置“化合物+熒光探針(無酶)”對照孔,排除假陽性。
六、文獻參考
Murai J., et al., 2014 Molecular Cancer Therapeutics 13: 433-443
Murai J., et. al., 2012 Cancer Research 72: 5588-5599
Zandarashvili L., et al., 2020 Science 368(6486): 6367
Marques M., et al., 2019 Oncogene 38 (12): 2177-2191.

微信掃碼在線客服