PRODUCT CENTER
特色產(chǎn)品當(dāng)前位置:首頁(yè) > 特色產(chǎn)品
研究目的:
Wieslab 補(bǔ)體系統(tǒng)經(jīng)典途徑是一種酶免疫測(cè)定法,用于定性或半定量測(cè)定人血清中功能性經(jīng)典補(bǔ)體途徑,其結(jié)果不得用于臨床診斷或患者管理。
概述和解釋
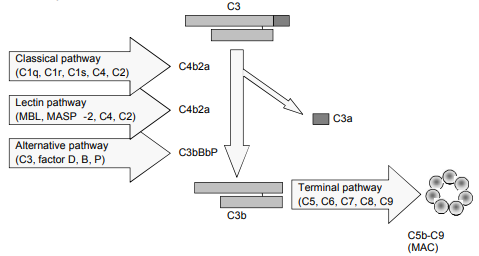
補(bǔ)體系統(tǒng)在慢性、自身免疫和感染性疾病中發(fā)揮著重要作用。補(bǔ)體激活有三個(gè)途徑(圖1),即經(jīng)典途徑、替代途徑和凝集素途徑。
補(bǔ)體活性受損會(huì)導(dǎo)致人類易患重復(fù)性暴發(fā)性或嚴(yán)重感染,并可能促進(jìn)自身免疫疾病的發(fā)展。補(bǔ)體的不適當(dāng)激活會(huì)導(dǎo)致慢性炎癥和組織損傷。
體外補(bǔ)體序列的激活導(dǎo)致補(bǔ)體成分的消耗,這反過(guò)來(lái)導(dǎo)致它們濃度的降低。因此,補(bǔ)體蛋白或補(bǔ)體活性的測(cè)定用于指示補(bǔ)體系統(tǒng)是否已被免疫和/或病理機(jī)制激活。當(dāng)懷疑補(bǔ)體激活性疾病或可能存在遺傳性缺陷時(shí),功能性和免疫化學(xué)補(bǔ)體測(cè)量都用于評(píng)估個(gè)體。通過(guò)功能性測(cè)定(如Wieslab 補(bǔ)體試劑盒)評(píng)估的補(bǔ)體活性水平考慮了成分的合成、降解和消耗速率,并提供了途徑完整性的度量,與免疫化學(xué)方法相對(duì),后者專門(mén)測(cè)量各種補(bǔ)體成分的濃度。
艾美捷WIESLAB補(bǔ)體系統(tǒng)經(jīng)典途徑(WIESLAB Complement System Classical Pathway)(#COMPLCP310)的測(cè)定原理:
Wieslab 補(bǔ)體經(jīng)典途徑測(cè)定結(jié)合了補(bǔ)體激活的溶血測(cè)定原理和使用特定于補(bǔ)體激活產(chǎn)生的新抗原的標(biāo)記抗體。產(chǎn)生的新抗原量與補(bǔ)體途徑的功能活性成正比。
在補(bǔ)體CP試劑盒中,微孔板條的孔被經(jīng)典途徑的特定激活劑包被。這與樣本稀釋緩沖液組成和血清稀釋水平相結(jié)合,確保只有經(jīng)典途徑被激活。
在孔中孵育稀釋的血清期間,補(bǔ)體通過(guò)特定包被被激活。然后洗滌孔,并使用特定的堿性磷酸酶標(biāo)記抗體檢測(cè)在MAC(膜攻擊復(fù)合物)形成期間形成的C5b-9新抗原上的C5b-9復(fù)合物。
在進(jìn)一步洗滌步驟后,通過(guò)與堿性磷酸酶底物溶液孵育獲得特定抗體的檢測(cè)。補(bǔ)體激活量與顏色強(qiáng)度相關(guān),并以吸光度(光密度(OD))來(lái)衡量。
樣本收集:
血液樣本應(yīng)使用無(wú)菌靜脈穿刺技術(shù)收集,并使用標(biāo)準(zhǔn)程序獲得血清。建議至少收集5毫升全血。讓血液在血清管中凝固60-65分鐘,室溫(20-25°C)。離心血液樣本,并將無(wú)細(xì)胞血清轉(zhuǎn)移到干凈的管中。血清必須正確處理以防止體外補(bǔ)體激活。血清應(yīng)密封在緊緊封閉的管中冷凍在-70°C或更低的溫度下,以便于長(zhǎng)期儲(chǔ)存或在干冰上運(yùn)輸。樣本不應(yīng)多次冷凍和解凍。
不要使用黃疸、乳糜和溶血的血清。不能使用熱滅活血清。
不能使用血漿。CLSI提供了儲(chǔ)存血液樣本的建議(血液樣本處理和處理程序的批準(zhǔn)標(biāo)準(zhǔn)-程序,H18A,1990年)。
試劑盒組件和試劑儲(chǔ)存:
一個(gè)框架,帶有無(wú)色分離孔(12x8),涂有人類IgM,密封在帶有干燥劑的鋁箔包裝中。
2 x 35毫升CP稀釋液(Dil CP),標(biāo)為藍(lán)色。
13毫升含有堿性磷酸酶標(biāo)記的C5b-9抗體的結(jié)合物(藍(lán)色)。
13毫升即用型底物溶液。
30毫升30倍濃縮的洗滌溶液。
0.2毫升陰性對(duì)照(NC),含有人血清(應(yīng)按個(gè)體血清樣本稀釋)。
凍干陽(yáng)性對(duì)照(PC),含有凍干人血清,需在0.2毫升蒸餾水中重組,見(jiàn)下文“陽(yáng)性對(duì)照的重組”。
凍干活性對(duì)照(AC),用于半定量應(yīng)用,含有凍干人血清(與PC來(lái)源不同),見(jiàn)“半定量應(yīng)用程序下的活性對(duì)照重組”。
陽(yáng)性對(duì)照和活性對(duì)照應(yīng)到達(dá)后儲(chǔ)存在-20°C。
請(qǐng)注意:AC的重組體積在分析證書(shū)(CoA)(XXX微升)和AC標(biāo)簽上標(biāo)明。
試劑盒中的所有試劑都已準(zhǔn)備好使用,除了洗滌溶液和對(duì)照品。試劑應(yīng)儲(chǔ)存在2-8°C,除了陽(yáng)性對(duì)照和活性對(duì)照。重組的陽(yáng)性對(duì)照和活性對(duì)照應(yīng)儲(chǔ)存在-70°C,并且只能解凍一次。
所需但未提供的物料或設(shè)備:
帶有405納米濾光片的微孔板讀取器。
帶有一次性吸頭的精密移液器。
用于條帶的清洗器、吸水紙、管子和一個(gè)計(jì)時(shí)器。
程序 定性應(yīng)用:
僅取出所需數(shù)量的孔,小心重新密封鋁箔包裝。在分析前讓所有溶液平衡至室溫(20-25°C)。不要在不同批次的試劑之間混合。
洗滌溶液的準(zhǔn)備
如果濃縮洗滌溶液瓶中觀察到鹽晶體,將瓶子置于37°C水浴中直到晶體溶解,然后再稀釋洗滌溶液。
將30毫升30倍濃縮洗滌溶液稀釋在870毫升蒸餾水中。當(dāng)儲(chǔ)存在2-8°C時(shí),稀釋后的洗滌溶液穩(wěn)定直到試劑盒的有效期。
預(yù)期結(jié)果:
當(dāng)發(fā)現(xiàn)補(bǔ)體成分或補(bǔ)體功能水平降低時(shí),臨床醫(yī)生會(huì)考慮缺陷或正在進(jìn)行的免疫過(guò)程,導(dǎo)致成分分解增加和補(bǔ)體水平降低。
對(duì)于定性測(cè)定,正常分布已確定為陽(yáng)性對(duì)照的69-129%,見(jiàn)表1。在此范圍內(nèi)的結(jié)果表明經(jīng)典途徑的功能正常。建議每個(gè)實(shí)驗(yàn)室確認(rèn)或建立自己服務(wù)人群的參考范圍。
低于69-129%范圍的值表明要么由于經(jīng)典補(bǔ)體途徑容量的消耗導(dǎo)致增加的激活,要么基因決定的低活性。
低于5%的值強(qiáng)烈表明由于過(guò)度激活或經(jīng)典途徑的遺傳性缺陷導(dǎo)致的完全缺乏。為了確定導(dǎo)致活性降低的補(bǔ)體因子,需要進(jìn)一步分析補(bǔ)體蛋白。
陰性結(jié)果,即懷疑缺乏,應(yīng)始終通過(guò)測(cè)試新的、仔細(xì)處理的樣本來(lái)驗(yàn)證,以確保沒(méi)有發(fā)生體外補(bǔ)體激活。
補(bǔ)體水平的增加通常是急性期反應(yīng)的非特異性表現(xiàn)。
Wieslab 補(bǔ)體系統(tǒng)經(jīng)典途徑可以幫助檢測(cè)與經(jīng)典途徑相關(guān)的補(bǔ)體缺陷,如下表所示:使用Wieslab 補(bǔ)體系統(tǒng)篩選,可以更完整和深入地功能性評(píng)估所有三個(gè)補(bǔ)體途徑。
WIESLAB補(bǔ)體系統(tǒng)經(jīng)典途徑文獻(xiàn)參考:
Walport M. Complement (First of two parts). N Engl J Med 2001; 344:1058-66.
Walport M. Complement (Second of two parts). N Engl J Med 2001; 344:1140-44.
Roos A et al. Functional characterization of the lectin pathway of complement in human serum.
Mol Immunol 2003; 39:655-68.
Fredriksson GN et al. New procedure for detection of complement deficiency by
ELISA. Analysis of activation pathways and circumvention of rheumatoid factor influence.
J Immunol Meth 1993; 166:263-70.
Seelen MA et al. Functional analysis of the classical, alternative and MBL pathways of the
complement system: standardization and validation of a simple ELISA. J Immunol Meth 2005;
296:187-98.
Salvador-Morales C, Sim RB. Handbook of Immunological Properties of Engineered
Nanomaterials. 2013, 1st Ed, World Scientific Publishing (ISBN: 978-4390-25-5).
Tudoran R & Kirschfink M. Modern Complement analysis: indications, methods and outlook.
LaboratoriumsMedizin 2012; 36(3):--.
Botto M et al. Complement in human disease: Lessons from complement deficiencies. Mol
Immunol 2009; 46:2774-83.
Mollnes TE et al. Complement analysis in the 21st century. Mol Immunol 2007; 44:3838-49.
Nilsson B, Nilsson Ekdahl K. Complement Diagnostics: Concepts, Indications, and Practical
Guidelines. Clin Develop Immunol; 2012, Art ID 962702

微信掃碼在線客服