PRODUCT CENTER
特色產(chǎn)品當前位置:首頁 > 特色產(chǎn)品
肺炎支原體是一種病原體,其臨床表現(xiàn)范圍從無癥狀到明顯的肺炎。癥狀在暴露后6到32天開始,包括頭痛、不適、咳嗽、喉嚨痛和發(fā)燒。病程可能持續(xù)幾天到一個月甚至更長時間。通過ELISA檢測到M. pneumoniae IgM抗體或特異性IgG抗體的顯著增加,是適當臨床環(huán)境中近期感染的有力證據(jù)。通常在臨床發(fā)病后1周特異性IgM抗體顯著增加,第二周特異性IgG水平上升。然而,M. pneumoniae IgM在感染后可以持續(xù)存在超過兩年,因此,特異性IgM的檢測并不準確表示感染時間。初次感染和再感染可以通過初次感染中存在特異性IgA和特異性IgM的升高,以及再感染中存在特異性IgA而無特異性IgM的存在來區(qū)分。通常,如果在發(fā)病后10-20天收集的血清中缺少特異性IgM,則強烈表明不是由M. pneumoniae引起的原發(fā)性肺炎。
Calbiotech-肺炎支原體(肺炎支原體)IgG ELISA測試系統(tǒng)是一種酶聯(lián)免疫吸附試驗(ELISA),用于檢測人血清或血漿中肺炎支原體的IgG類抗體。
艾美捷Calbiotech肺炎支原體IgG ELISA(MP020G)檢測原理:
將稀釋的患者血清加入到涂有純化抗原的孔中。如果存在IgG特異性抗體,它會與抗原結(jié)合。所有未結(jié)合的物質(zhì)都被洗去,然后加入酶結(jié)合物與存在的抗體-抗原復合物結(jié)合。過量的酶結(jié)合物被洗掉,然后加入底物。孵育板以允許酶水解底物。產(chǎn)生的色澤強度與樣本中IgG特異性抗體的數(shù)量成正比。
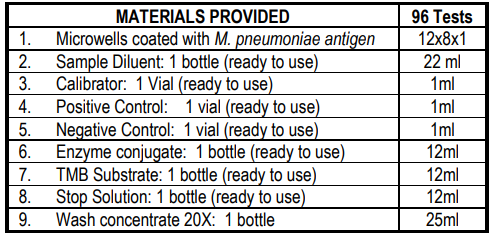
測定程序:
將所有樣本和試劑盒組分置于室溫(20-25°C)并輕輕混合。
1. 將所需數(shù)量的包被條放入支架中。
2. 陰性對照、陽性對照和校準品已準備好使用。通過向200微升樣品稀釋液中加入10微升樣本來準備測試樣品的1:21稀釋。混合均勻。
3. 向相應的孔中分發(fā)100微升稀釋血清、校準品和對照品。對于試劑空白,在1A孔位分發(fā)100微升樣品稀釋液。輕敲支架以去除液體中的空氣泡,并混合均勻。在室溫下孵育20分鐘。
4. 清除所有孔中的液體。用300微升1X洗滌緩沖液洗孔三次。用吸收紙或紙巾拍干。
5. 向每個孔中分發(fā)100微升酶結(jié)合物,并在室溫下孵育20分鐘。
6. 清除所有孔中的酶結(jié)合物。用300微升1X洗滌緩沖液洗孔三次。用吸收紙或紙巾拍干。
7. 向每個孔中分發(fā)100微升TMB底物,并在室溫下孵育10分鐘。
8. 加入100微升終止溶液。
9. 在15分鐘內(nèi)使用ELISA讀數(shù)器讀取450納米處的光密度(O.D.)。建議使用參考濾光片600-650納米的雙波長。
肺炎支原體IgG ELISA文獻參考:
1. Quinn TC. Diagnosis of atypical pneumonias: Legionella, Chlamydia, and Mycoplasma infections. Ann Intern Med1996;124:591-4.
2. Cimolai N, Cheong ACH. An assessment of a new diagnostic indirect enzyme immunoassay for the detection ofanti-Mycoplasma pneumoniae IgM. Am J Clin Pathol 1996;105:205-9.
3. 5. Shearman MJ, Cubie HA, Inglis JM. Mycoplasma pneumoniae infection: early diagnosis by detection of specificIgM by immunofluorescence. Br J Biomed Sci 1993;50:305-8.
4. Lee SH, Charoenying S, Brennan T, Markowski M, Mayo DR. Comparative studies of three serologic methods forthe measurement of Mycoplasma pneumoniae antibodies. Am J Clin Pathol 1989;92:342-7.
5. Kenny GE, Kaiser GG, Cooney MK, Foy HM. Diagnosis of Mycoplasma pneumoniae pneumonia: sensitivities andspecificities of serology with lipid antigen and isolation of the organism on soy peptone medium for identification ofinfections. J Clin Microbiol 1990;28:2087- 93.
6. Aubert G, Pozzetto B, Gaudin OG, Hafid J, Mbida AD, Ros A. Evaluation of five commercial tests: complementfixation, microparticle agglutination, indirect immunofluorescence, enzyme-linked immunosorbent assay and latexagglutination, in comparison to immunoblotting for Mycoplasma pneumoniae serology. Ann Biol Clin 1992;50:593
7. Kok T, Mickan LD, Burrell CJ. Routine diagnosis of seven respiratory viruses and Mycoplasma pneumoniae byenzyme immunoassay. J Virol Methods 1994;50:87-100.
8. Kleemola M, R?ty R, Karjalainen J, Schuy W, Gerstenecker B, Jacobs E. Evaluation of an antigen-captureenzyme immunoassay for rapid diagnosis of Mycoplasma pneumoniae infection. Eur J Clin Microbiol Infect Dis1993;12:872-5.
艾美捷科技是Calbiotech的中國代理商,為科研工作者提供優(yōu)質(zhì)的產(chǎn)品與服務。

微信掃碼在線客服