TECHNICAL COLUMN
學(xué)習(xí)資源當(dāng)前位置:首頁 > 學(xué)習(xí)資源
胞葬作用 (Efferocytosis),即吞噬細(xì)胞對凋亡細(xì)胞的吞噬,相信大家都有了解過,今天通過了解胞葬作用中嗅覺階段、吞噬階段、消化階段。各階段的關(guān)鍵信號分子和相關(guān)信號通路可作為治療胞葬異常性疾病的藥物開發(fā)靶點,今天讓我們通過一篇發(fā)表于Nat Rev Drug Discov(IF:112.228)題為“Drugging the efferocytosis process: concepts and opportunities”的綜述文章,一探究竟。

人體每天大約有200-3000億個細(xì)胞主要通過半胱天冬酶依賴性細(xì)胞凋亡的死亡過程被更新,對于機(jī)體各種組織中的組織穩(wěn)態(tài)、胚胎發(fā)育、傷口愈合和炎癥消退至關(guān)重要。細(xì)胞死亡與凋亡細(xì)胞的高效吞噬作用高度結(jié)合,導(dǎo)致凋亡細(xì)胞很難被觀察到。而凋亡細(xì)胞清除失敗或缺陷可能會導(dǎo)致多種病理狀況,這也為靶向胞葬作用過程的各個步驟發(fā)揮抗炎作用提供可能。
胞葬作用有兩個好處:
一是快速去除凋亡細(xì)胞可防止它們繼發(fā)壞死,在那里它們可能會釋放誘發(fā)炎癥的潛在毒性細(xì)胞內(nèi)物質(zhì);
二是吞噬細(xì)胞通過增加抗炎介質(zhì)的分泌和上調(diào)促修復(fù)轉(zhuǎn)錄程序,轉(zhuǎn)變?yōu)楦按俜直媛省钡谋硇停沟皿w內(nèi)數(shù)十億死亡細(xì)胞以一種避免炎癥和非免疫原性的方式被清除。
胞葬作用步驟及治療前景
胞葬受多因素影響,多個步驟參與其中,包括“嗅覺階段”,在此期間吞噬細(xì)胞“感知”凋亡細(xì)胞的存在并定位它們。其次是“進(jìn)食階段”,此時凋亡細(xì)胞上的配體與吞噬細(xì)胞上的吞噬細(xì)胞受體結(jié)合,特異性識別和攝取垂死的細(xì)胞。第三是“消化階段”,處理攝入死亡細(xì)胞及其內(nèi)容物。
嗅覺階段
“find me”信號:
凋亡細(xì)胞:核苷酸(ATP、UTP)、LPC、S1P、CX3CL1
吞噬細(xì)胞:G2A、CX3CR1、LRP1、SRB1、P2Y2
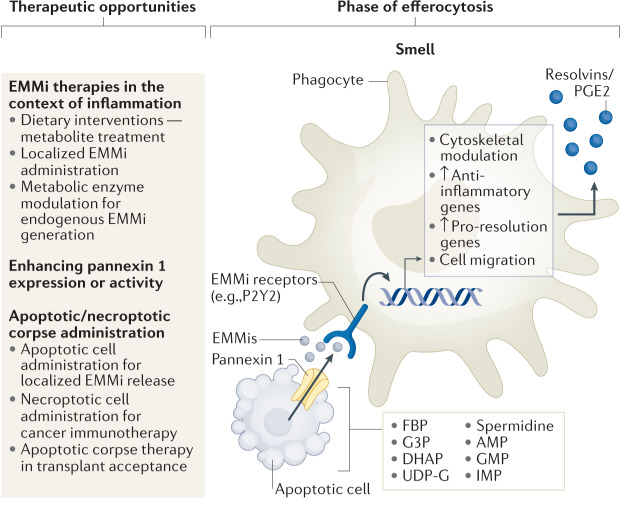
凋亡細(xì)胞釋放可溶性介質(zhì),包括多個“識我”信號,具有雙重作用,一方面作為吞噬細(xì)胞向凋亡細(xì)胞遷移的吸引信號;另一方面通過調(diào)節(jié)吞噬細(xì)胞骨架,增強(qiáng)吞噬受體的表達(dá),為吞噬做準(zhǔn)備(圖1)。
少量凋亡細(xì)胞內(nèi)核苷酸(<1%)的調(diào)節(jié)釋放可以作為單核細(xì)胞/巨噬細(xì)胞向凋亡細(xì)胞遷移的有效誘導(dǎo)劑,并促進(jìn)組織附近的抗炎基質(zhì)。最近研究表明,pannexin 通道介導(dǎo)T細(xì)胞釋放ATP和AMP,隨后轉(zhuǎn)化為腺苷,可以抑制氣道炎癥。凋亡細(xì)胞在凋亡早期主動釋放>100種代謝物,這些代謝物作為準(zhǔn)備信號反過來誘導(dǎo)吞噬細(xì)胞和鄰近細(xì)胞的轉(zhuǎn)錄變化,被鑒定為誘導(dǎo)與炎癥消退和組織修復(fù)相關(guān)的基因表達(dá)。
治療前景:代謝物中的一小部分可以被用作“藥物”來誘導(dǎo)促修復(fù)和抗炎基因轉(zhuǎn)錄程序。通過pannexin通道促進(jìn)AMP、其他核苷酸或代謝物的調(diào)節(jié)釋放是一種潛在的藥物靶向策略,如“體外光分離療法”(ECP)用于抑制系統(tǒng)性紅斑狼瘡(SLE)和關(guān)節(jié)炎的炎癥以及移植排斥反應(yīng);暴露于供體凋亡細(xì)胞的移植小鼠的排異反應(yīng)大大降低。
進(jìn)食階段
“eat me”信號:
凋亡細(xì)胞:PtdSer(PS)、氧化磷脂、內(nèi)質(zhì)網(wǎng)駐留鈣蛋白
吞噬細(xì)胞受體:TAM(Axl、Tyro3、MerTK)、TIM、TG2
“don't eat me”信號:
凋亡細(xì)胞:CD47、CD31
吞噬細(xì)胞受體:SIRPα
橋接分子:MFGE8、GAS6、ProS、血清補(bǔ)體C1q、Thbs1、AnxⅠ
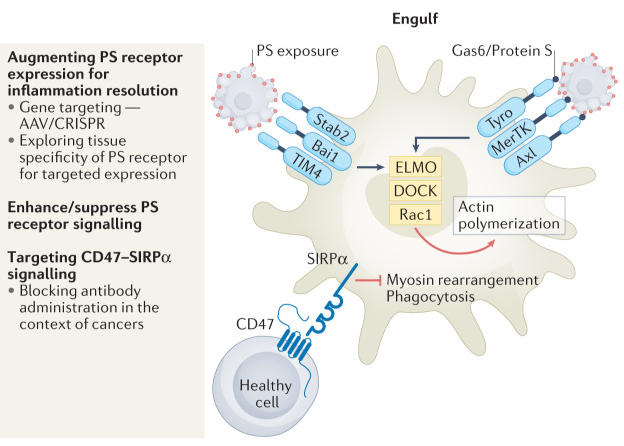
凋亡細(xì)胞表面“吃我”信號被吞噬細(xì)胞特異性受體識別,觸發(fā)一系列復(fù)雜的細(xì)胞骨架重排,從而促進(jìn)細(xì)胞吞噬“廢物”,如吞噬細(xì)胞直接或間接識別凋亡細(xì)胞的磷脂酰絲氨酸(PS)受體。細(xì)胞上暴露“不要吃我”信號有助于避免細(xì)胞吞噬,現(xiàn)已經(jīng)發(fā)現(xiàn)多種“不要吃我”分子,包括CD47和CD24(圖2)。
治療前景:多樣性PS受體參與多種病理過程,使其成為有吸引力的治療靶點。PS受體信號傳導(dǎo)的小分子抑制劑作為癌癥治療藥物正處于臨床試驗的后期階段。CD47與巨噬細(xì)胞上的SIRPα結(jié)合,通過募集SHP1/2抑制非肌肉肌球蛋白IIA來抑制吞噬作用,可依此作為抗癌免疫新療法的探索。單克隆抗體阻斷CD24–Siglec10(腫瘤相關(guān)巨噬細(xì)胞上的唾液酸結(jié)合免疫球蛋白樣lection 10)相互作用可以增加對腫瘤細(xì)胞的吞噬。
消化階段
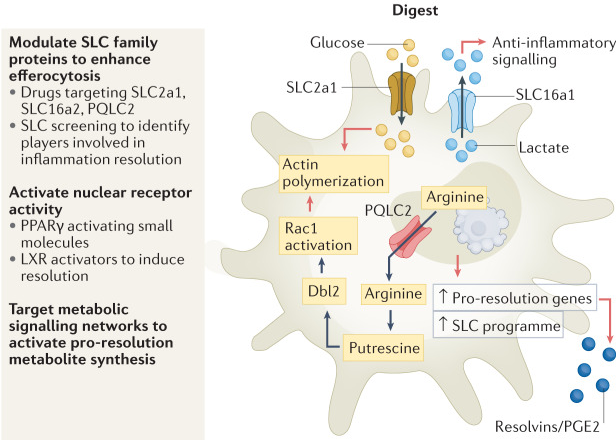
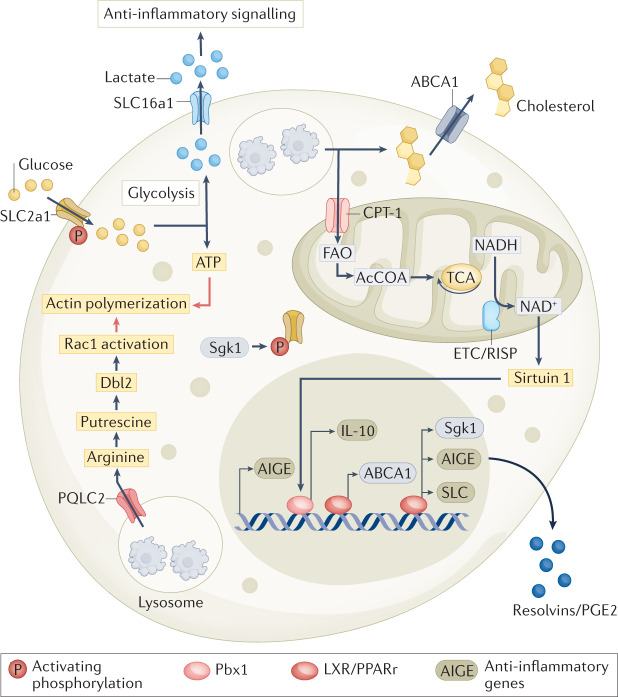
在細(xì)胞吞噬期間,細(xì)胞內(nèi)區(qū)室之間和細(xì)胞外空間的代謝物轉(zhuǎn)移可以改善抗炎基因表達(dá)和細(xì)胞吞噬的維持。吞噬細(xì)胞合成和分泌特殊的促溶解介質(zhì)(SPM)是調(diào)節(jié)細(xì)胞吞噬作用抗炎功能的另一途徑。吞噬細(xì)胞需要管理其體積和表面積來“包容”攝入“貨物”的多少,且攝入的“貨物”含有膜、膽固醇、蛋白質(zhì)、核酸等,這些高代謝負(fù)擔(dān)需要被代謝、被排泄或重新進(jìn)入吞噬細(xì)胞的代謝通量循環(huán)。最近的研究還表明,吞噬細(xì)胞內(nèi)的線粒體動力學(xué)可能在調(diào)節(jié)其體內(nèi)平衡和連續(xù)性中發(fā)揮重要作用(圖3、4)。
治療前景:人類慢性肉芽腫病患者單核細(xì)胞的PPARγ已被證明可以促進(jìn)胞吐作用(通過增加PS受體表達(dá))并誘導(dǎo)抗炎基因表達(dá);吞噬細(xì)胞的連續(xù)吞噬作用受阻時,增強(qiáng)SLC家族成員或溶酶體精氨酸轉(zhuǎn)運蛋白Pqlc2活性,可以在體外和體內(nèi)驅(qū)動持續(xù)的吞噬作用。利用細(xì)胞凋亡“貨物”的攝入觸發(fā)代謝重編程,幫助吞噬細(xì)胞抑制炎癥信號的特點,將免疫行為與代謝通量聯(lián)系起來的復(fù)雜蛋白質(zhì)相互作用網(wǎng)絡(luò)已成為高度優(yōu)先的藥物靶點。
胞葬作用涉及高度組織特異性PS受體和凋亡細(xì)胞負(fù)荷,是細(xì)胞更新普遍存在的現(xiàn)象。靶向胞葬藥物已逐漸走進(jìn)醫(yī)學(xué)研究者視野,在炎癥、動脈粥樣硬化、糖尿病以及衰老中具有極大的治療潛力。然而明確靶向疾病相關(guān)組織細(xì)胞受體以及冗雜的轉(zhuǎn)運蛋白體系是一個極大挑戰(zhàn),如癌癥中胞葬的“正常”作用、結(jié)核分枝桿菌感染后胞葬的細(xì)菌傳播等均限制了靶向治療的進(jìn)展。這需要多學(xué)科組合研究胞葬作用的動態(tài)過程,提高靶向胞葬作用藥物聯(lián)合治療相關(guān)疾病的可能性。
參考文獻(xiàn):Mehrotra P, Ravichandran KS. Drugging the efferocytosis process: concepts and opportunities. Nat Rev Drug Discov. 21(8), 601-620 (2022).

微信掃碼在線客服