TECHNICAL COLUMN
學(xué)習(xí)資源當(dāng)前位置:首頁 > 學(xué)習(xí)資源
細(xì)胞核一直被認(rèn)為是代謝惰性的,通過細(xì)胞質(zhì)中的供應(yīng)鏈進(jìn)口其所有需求,研究人員通過實(shí)驗(yàn),使用一種常見的化療藥物——依托泊苷,在人類細(xì)胞系中誘導(dǎo)DNA損傷。研究人員觀察到,細(xì)胞呼吸酶(活性氧的主要來源)在DNA損傷的情況下從線粒體轉(zhuǎn)移到細(xì)胞核。這一發(fā)現(xiàn)代表了細(xì)胞生物學(xué)的范式轉(zhuǎn)變,因?yàn)樗砻骷?xì)胞核具有代謝活性。
近日,有研究表明,細(xì)胞核的代謝是活躍的,細(xì)胞酶在受到損傷時(shí)保護(hù)DNA的完整性。這種對細(xì)胞代謝的理解的轉(zhuǎn)變可以為癌癥治療提供新的策略,因?yàn)榘┘?xì)胞經(jīng)常劫持代謝過程以促進(jìn)其生長。
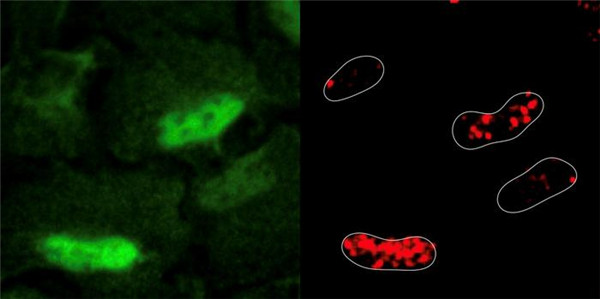
一個(gè)典型的人體細(xì)胞是新陳代謝活躍的,通過化學(xué)反應(yīng)將營養(yǎng)物質(zhì)轉(zhuǎn)化為能量和維持生命的有用產(chǎn)品。這些反應(yīng)還會產(chǎn)生活性氧,這是一種危險(xiǎn)的副產(chǎn)物,比如過氧化氫,它會破壞DNA的組成部分,就像氧氣和水腐蝕金屬并形成鐵銹一樣。就像建筑物因銹蝕的累積效應(yīng)而倒塌一樣,活性氧威脅著基因組的完整性。
人們認(rèn)為,細(xì)胞通過在細(xì)胞核外、細(xì)胞質(zhì)和線粒體內(nèi)進(jìn)行代謝活動來微妙地平衡它們的能量需求,避免破壞DNA。抗氧化酶的作用是在活性氧到達(dá)DNA之前將其清除,這是一種防御策略,可以保護(hù)大約30億個(gè)核苷酸免受潛在的災(zāi)難性突變。如果DNA損傷無論如何發(fā)生,細(xì)胞會暫時(shí)停止并進(jìn)行修復(fù),合成新的構(gòu)建塊并填補(bǔ)空白。
盡管細(xì)胞代謝在維持基因組完整性方面發(fā)揮著核心作用,但目前還沒有關(guān)于代謝擾動如何影響DNA損傷和修復(fù)過程的系統(tǒng)、公正的研究。這對癌癥等疾病尤其重要,因?yàn)樗鼈兡軌蚪俪执x過程以實(shí)現(xiàn)不受約束的生長。
由巴塞羅那基因組調(diào)控中心(CRG)的Sara Sdelci和維也納奧地利科學(xué)院分子醫(yī)學(xué)研究中心和維也納醫(yī)科大學(xué)的Joanna Loizou領(lǐng)導(dǎo)的一個(gè)研究小組通過開展各種實(shí)驗(yàn)來確定哪些代謝酶和過程對細(xì)胞的DNA損傷反應(yīng)至關(guān)重要,從而解決了這一挑戰(zhàn)。研究結(jié)果發(fā)表在今天的《Molecular Systems Biology》雜志上。
研究人員通過實(shí)驗(yàn),使用一種常見的化療藥物——依托泊苷,在人類細(xì)胞系中誘導(dǎo)DNA損傷。依托泊苷的工作原理是破壞DNA鏈,阻斷一種幫助修復(fù)損傷的酶。令人驚訝的是,誘導(dǎo)DNA損傷導(dǎo)致活性氧在細(xì)胞核內(nèi)產(chǎn)生和積累。研究人員觀察到,細(xì)胞呼吸酶(活性氧的主要來源)在DNA損傷的情況下從線粒體轉(zhuǎn)移到細(xì)胞核。
這一發(fā)現(xiàn)代表了細(xì)胞生物學(xué)的范式轉(zhuǎn)變,因?yàn)樗砻骷?xì)胞核具有代謝活性。“哪里有煙哪里就有火,哪里有活性氧就有代謝酶在起作用。從歷史上看,我們一直認(rèn)為細(xì)胞核是一種代謝惰性的細(xì)胞器,它從細(xì)胞質(zhì)中進(jìn)口所有需要的東西,但我們的研究表明,細(xì)胞中存在另一種類型的代謝,并且在細(xì)胞核中發(fā)現(xiàn),”該研究的通訊作者、基因組調(diào)控中心的組長Sara Sdelci博士說。
研究人員還使用CRISPR-Cas9識別了在這種情況下對細(xì)胞存活很重要的所有代謝基因。這些實(shí)驗(yàn)表明,細(xì)胞命令PRDX1酶(一種通常也存在于線粒體中的抗氧化酶)前往細(xì)胞核,清除存在的活性氧,以防止進(jìn)一步的損傷。PRDX1還被發(fā)現(xiàn)通過調(diào)節(jié)細(xì)胞中天冬氨酸的可用性來修復(fù)損傷,天冬氨酸是一種對合成核苷酸(DNA的組成部分)至關(guān)重要的原料。
“PRDX1就像一個(gè)機(jī)器人泳池清潔工。眾所周知,細(xì)胞利用它來保持內(nèi)部“清潔”,防止活性氧的積累,但以前從未在核水平上使用過。這證明,在危機(jī)狀態(tài)下,細(xì)胞核通過挪用線粒體機(jī)制作出反應(yīng),并建立緊急快速工業(yè)化政策,”Sdelci博士說。
這些發(fā)現(xiàn)可以指導(dǎo)未來的癌癥研究方向。一些抗癌藥物,如本研究中使用的依托泊苷,通過破壞腫瘤細(xì)胞的DNA和抑制修復(fù)過程來殺死腫瘤細(xì)胞。如果累積了足夠的損傷,癌細(xì)胞就會啟動一個(gè)自我毀滅的過程。
在他們的實(shí)驗(yàn)中,研究人員發(fā)現(xiàn),敲除對細(xì)胞呼吸至關(guān)重要的代謝基因——從氧氣和營養(yǎng)物質(zhì)中產(chǎn)生能量的過程——會使正常的健康細(xì)胞對依托波苷產(chǎn)生抵抗力。這一發(fā)現(xiàn)很重要,因?yàn)樵S多癌細(xì)胞是糖酵解的,這意味著即使在氧氣存在的情況下,它們也會產(chǎn)生能量,而不進(jìn)行細(xì)胞呼吸。這意味著依托泊苷和其他具有類似機(jī)制的化療在治療糖酵解性腫瘤方面可能效果有限。
該研究的作者呼吁探索新的策略,例如將依托泊苷與藥物聯(lián)合使用的雙重治療,也可以促進(jìn)活性氧的產(chǎn)生,以克服耐藥性,更快地殺死癌細(xì)胞。他們還假設(shè),將依托泊苷與核苷酸合成過程的抑制劑結(jié)合可以通過阻止DNA損傷的修復(fù)和確保癌細(xì)胞正確地自我毀滅來增強(qiáng)藥物的作用。
Joanna Loizou博士,通訊作者和維也納醫(yī)科大學(xué)分子醫(yī)學(xué)中心的組長,強(qiáng)調(diào)了采用數(shù)據(jù)驅(qū)動方法來發(fā)現(xiàn)新的生物過程的價(jià)值。“通過使用無偏見的技術(shù),如CRISPR-Cas9篩選和代謝組學(xué),我們了解了DNA修復(fù)和代謝這兩個(gè)基本細(xì)胞過程是如何交織在一起的。我們的研究結(jié)果揭示了針對這兩種癌癥途徑如何改善患者的治療效果。”
文獻(xiàn)參考:
A metabolic map of the DNA damage response identifies PRDX1 in the control of nuclear ROS scavenging and aspartate availability

微信掃碼在線客服