TECHNICAL COLUMN
學習資源
凝膠內(nèi)蛋白的顯色
蛋白顯色的階段非常重要,可以知道蛋白遷移的是否均勻、平坦。如果分離后的蛋白需要轉膜,就用銅染,因為考馬斯藍染色是不可逆的。 考馬斯藍染色只用來檢測轉移的有效性,或者蛋白不需要轉膜時,只用于觀測蛋白 SDS-PAGE 分離的結果。
1.a) 考馬斯藍染色
電源關閉,分離的蛋白帶就會擴散,因為蛋白在溶液中是可溶的,為了防止擴散,凝膠中加入 40% 雙蒸水、10% 醋酸、50% 甲醇,能使蛋 白質沉淀(變成不溶性的)。在上述溶液中加入 0.25% 考馬斯亮藍 R-250 使被固定的蛋白染色,在搖床上保持搖動,室溫,4 小時至過夜。 轉移凝膠至 67.5% 雙蒸水、7.5% 醋酸、25% 甲醇混合物中(染料混合物保存起來,可多次重復使用)潤洗,一直在搖床上震搖,中間更換 潤洗液,直到洗去多余染料。染料不會結合到丙烯酰胺上,凝膠背景清晰,凝膠中的蛋白條帶染成深藍色。
2.b) 銅染法
電泳凝膠用蒸餾水清洗數(shù)秒鐘(最多 30 秒),然后轉移至 0.3 M CuCl2 溶液中染色 5-15 分鐘,再用去離子水洗一次,在暗背景下觀察,在 藍色膠背景下蛋白出現(xiàn)透明條帶。
將膠置于 0.1- 0.25 M Tris/0.25 M EDTA pH 8.0 緩沖液中漂洗凝膠完全脫色,根據(jù)廠家說明再置于電轉緩沖液中開始轉膜。
蛋白轉膜
1.詳細的轉膜操作可以在電轉儀廠家的網(wǎng)頁上找到,不同的系統(tǒng)操作也有區(qū)別。蛋白從凝膠至膜的轉移應用的原理是電荷在電場中的遷移。
2.轉膜方式分為半干轉移和濕轉移兩種,半干式轉膜速度快,而濕式轉膜不會因為膜的干燥而失敗,因此成功率高并特別適合用于分子量大 于100kDa 的蛋白。兩種轉膜方式都是膜緊貼凝膠,位于兩層吸收材料之間,固體夾板夾在外面以保證膜和凝膠的緊密接觸。
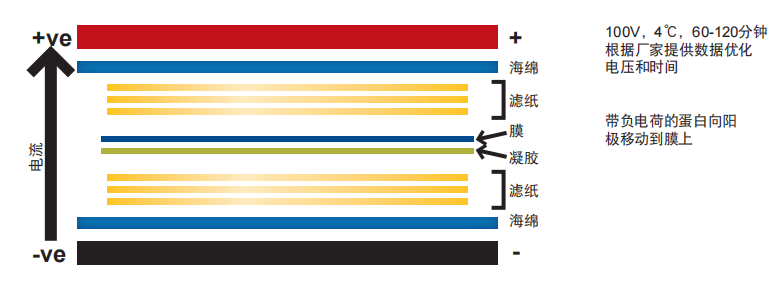
3.濕式轉膜中膜和凝膠的三明治結構位于濾紙和海綿體之間(海綿/紙/膠/膜/紙/海綿),全部緊密排列,特別是膠/膜之間不能留有氣泡。整 個三明治結構浸泡在轉移緩沖液中,然后施加電場。帶負電荷的蛋白向陽極移動。但膜阻擋了它們,并與其進行結合,從而阻止了它們的 繼續(xù)移動。凝膠一般在 100V 條件下運行 1~2 小時,時間和電壓可以優(yōu)化,我們推薦根據(jù)廠家的說明進行操作。
4.標準的濕轉緩沖液和電泳緩沖液一樣,為不含 SDS 的 1X Tris-gly 緩沖液,加入甲醇至終濃度 20%。如果轉膜的蛋白分子量大于 80kDa, 則推薦加入 SDS 使之終濃度為 0.1%。
5.半干式轉膜中,三明治結構紙/凝膠/膜/紙用轉移緩沖液浸濕,直接置于電轉儀的正負極之間。在進行轉移時,要注意一定要使膜緊貼陽極 而膠緊貼陰極。所用的電轉緩沖液中 Tris 和甘氨酸的比例不一定和濕轉的相同,需參考廠家的儀器說明書。標準配方是:48mM Tris、 39mM 甘氨酸、0.04% SDS、20% 甲醇。
6.兩類膜可供選擇:硝酸纖維素膜和 PVDF 膜(正電荷尼龍膜)。PVDF 膜需要小心地進行前處理:剪出大小合適的膜,在甲醇中浸泡 1-2 分 鐘,再孵育于冰冷的電轉緩沖液中5分鐘。膠也需在冰冷的電轉緩沖液中平衡 3-5 分鐘,否則轉膜時會起皺導致條帶變形。
大蛋白和小蛋白轉膜時的注意事項
電轉移緩沖液中 SDS 與甲醇的平衡、蛋白大小、膠濃度都會影響轉膜效果,如下調(diào)整可以增加轉膜效果。
大蛋白(大于100 kDa)
1.對于大蛋白而言,其在凝膠電泳分離遷移較慢,而從凝膠轉出也非常慢,因此對于這種大分子量蛋白應該用低濃度的凝膠,8%
或更低, 但因低濃度的膠非常易碎,所以操作時需十分小心。
2.大蛋白易在凝膠里形成沉淀,從而影響轉膜。轉膜時在電轉移緩沖液加入 SDS 至終濃度 0.1%,避免出現(xiàn)這種情況。甲醇易使
SDS 從蛋 白上脫失,因此相應降低甲醇的濃度至 10% 或更低,以防止蛋白沉淀。
3.降低電轉移緩沖液中甲醇的比例,這樣可以促進凝膠的膨脹,更易于大蛋白的轉出。
4.只有使用硝酸纖維素膜時,甲醇才是必需的。如果是 PVDF 膜,甲醇可以不必加入電轉移緩沖液中,但轉膜前 PVDF 需用甲醇活化。
5.選擇濕式,4℃ 轉膜過夜,以取代半干式轉膜。
小蛋白(小于100 kDa)
1.SDS 阻止蛋白與膜的結合,小蛋白更是如此。因此,對于小分子的蛋白,電轉移緩沖液中可以不加 SDS。
2.保持 20% 的甲醇濃度對于大于 500kDa 的蛋白,請參考下述文獻:
Bolt and Mahoney, High-efficiency blotting of proteins of diverse sizes following sodium dodecyl sulfate–polyacrylamide,gel electrophoresis. Analytical Biochemistry
247, 185–192 (1997).
更多的轉膜技巧:
避免手指直接接觸膜,應使用鑷子,手指上的油脂與蛋白會封閉轉膜效率并易產(chǎn)生背景污斑。
在濾紙間排列凝膠和膜時,盡量用移液器或 15ml 試管趕除膠與膜之間的氣泡,或在轉移緩沖液中進行以防止氣泡產(chǎn)生,請戴手套!
確認裁剪的膜和濾紙與凝膠尺寸相同,邊緣太大會導致在進行半干式轉膜時電流不能通過膜。
雞抗體易與 PVDF 膜和其它尼龍膜結合,導致高背景,請?zhí)鎿Q成硝酸纖維素膜以降低背景。
膜上蛋白的顯像:麗春紅
為檢測轉膜是否成功,用 TBST 洗膜(TBST 溶液的配制詳見 71 頁緩沖液章節(jié))。準備貯備液:2% 麗春紅 S 溶于 30% 三氯乙酸和
30% 磺 基水楊酸,室溫下震搖 5 分鐘。1:10 稀釋貯備液。
然后將膜浸泡在水中直至水變清且蛋白條帶清晰。
用 TBST 或水重復洗膜直至膜完全脫色,PVDF 膜需用甲醇活化后再用 TBST 洗。
膜的封閉
有兩種傳統(tǒng)封閉液:脫脂奶粉或 BSA(Cohn 因子 V),脫脂奶粉成本低但不能用于磷酸化蛋白(因脫脂奶粉含有酪蛋白,該蛋白本身就是 一種磷酸化蛋白,會結合磷酸化特異性抗體而易產(chǎn)生高背景。)
為防止一抗或/和二抗與膜的非特異性結合,需要進行膜的封閉。
某些抗體用 BSA 封閉時可能會產(chǎn)生比脫脂奶粉更強的信號,請仔細閱讀說明書,以確定有無特殊封閉膜方法。
用封閉緩沖液封閉 1 小時,4°C 震搖,封閉后用 TBST 洗 5 秒。
一抗的孵育
孵育緩沖液
按抗體說明書建議的稀釋倍數(shù),用 TBST 稀釋一抗。如果說明書沒有建議稀釋倍數(shù),則參照一般推薦的稀釋倍數(shù) (1:100-1:3000)進行預試驗,根 據(jù)試驗結果選擇合適稀釋倍數(shù),一抗?jié)舛冗^高會導致產(chǎn)生非特異性條帶。
某些實驗室傳統(tǒng)上在封閉液中孵育抗體,而有些實驗室用不含封閉劑的 TBST 來孵育抗體,結果因抗體而異,有時兩者結果相同,有時結果 不同。
如果不存在高背景的問題,某些抗體用含低濃度 (0.5 – 0.25%) 脫脂奶粉或 BSA 的封閉液甚至二者都不含的封閉液來稀釋,可產(chǎn)生相對更強的信號條帶。
孵育時間
一抗的孵育時間可從幾小時至過夜(一般不超過 18 小時)不等,具體取決于抗體與蛋白的親和性和蛋白的豐度,建議使用較高的抗體稀釋 倍數(shù)和較長的孵育時間來保證特異性結合。
孵育溫度
如果在封閉液中孵育過夜,應在 4oC 進行,否則污染會導致蛋白降解(特別是磷酸基團)。孵育一抗時需保持適當?shù)膿u動使之均勻覆蓋膜,防 止結合不均勻。
二抗的孵育
一抗孵育結束后,用 TBST 搖動洗膜數(shù)次,每次 5 分鐘或更長,去除殘留的一抗。
孵育緩沖液和稀釋:
按說明書推薦的倍數(shù)用 TBST 稀釋二抗,如果說明書沒有標出稀釋倍數(shù),則按常規(guī)的倍數(shù)稀釋 (1:1000- 1:20,000) 預實驗,二抗的濃度過高 也會導致非特異性條帶。
可以在封閉液中孵育二抗(和一抗),但可能在降低背景同時導致特異性條帶的信號也減弱,可能是封閉劑阻礙了抗體與靶蛋白的結合。
孵育時間和溫度:
室溫振蕩 1-2 小時。
標記物:推薦使用 HRP 標記二抗,不建議使用 AP(堿性磷酸酶)標記二抗,因其不夠靈敏。
顯色方法
檢測試劑盒:
HRP 標記二抗:傳統(tǒng)上使用 ECL 和 ECL+(自制或購買),推薦使用后者。對于新一代檢測儀器例如 Genegnome,請用儀器制造商推薦的試劑盒。
我們不推薦 ECL 或 BCIP/NBT 試劑盒,因為不夠靈敏。
X-ray 膠片:
傳統(tǒng)上使用手工曝光的方法,可控制 X-ray 膠片在曝光劑和定影劑的時間。而全自動 X-ray 膠片曝光器也已經(jīng)廣泛使用且操作簡便。
過度曝光的膠片不適合用于分析,因為不能判定相對蛋白量。
過度曝光導致全暗的背景沒有反差和/或產(chǎn)生大量的非特異性條帶。
數(shù)字圖像顯影:
新一代的膠片顯色方法是使用數(shù)碼相機在暗室中拍攝膜上的化學發(fā)光,將其轉成數(shù)字信號,再通過儀器自帶的軟件進行分析。
一系列的數(shù)字成像儀都已經(jīng)商品化。新一代數(shù)字成像儀不使用 HRP 標記抗體(即化學發(fā)光),如 STORM 分析儀只檢測熒光標記二抗, Odyssey 紅外線成像系統(tǒng)探測紅外線熒光。

微信掃碼在線客服