TECHNICAL COLUMN
學(xué)習資源
一、樣品準備
裂解緩沖液
準備凝膠電泳的樣品,需要對細胞和組織進行裂解以釋放目的蛋白,這些可溶性蛋白能夠穿過分離膠單獨移動。裂解緩沖液有很多種,但用 來做 WB試驗的僅有少數(shù)幾種。簡單來說,它們?nèi)芙獾鞍椎哪芰Σ煌惺榛蛩徕c和其他離子型去污劑的溶解能力最強。
有些購買的抗體能夠識別降解和變性蛋白質(zhì),因此應(yīng)該在降解和變性條件下使用該類抗體。需要注意的是一些抗體僅僅識別天然的、非變 性蛋白質(zhì),故不能識別經(jīng)去污劑(SDS、脫氧膽酸鹽、弱降解作用的 Triton X-100 和 NP40)作用的蛋白質(zhì)。
選擇裂解緩沖液首先要考慮選擇的抗體是否識別變性的樣品。如果不能,有關(guān)資料會列在抗體說明書上,應(yīng)該使用不含去污劑的緩沖液或者 是相對溫和的非離子型緩沖液(NP-40,吐溫 X-100)。
蛋白定位和裂解液的選擇
樣品類型 | 裂解液 |
全細胞 | NP-40或RIPA |
細胞質(zhì)(可溶性的) | Tris-HCI |
細胞質(zhì)(細胞骨架) | Tris-Triton |
膜結(jié)合部分 | NP-40或RIPA |
細胞核 | RIPA或核裂解液 |
線粒體 | RIPA或線粒體分離方案 |
*專門或主要表達在亞細胞結(jié)構(gòu)區(qū)域的蛋白在亞細胞裂解物中比在全細胞和組織裂解物中更為富集。這對于提取弱表達蛋白非常重要。例如, 相對于全細胞或全組織裂解物來說,核表達蛋白在細胞核裂解物總蛋白中占有相當大的比例,這樣凝膠條帶中可以載入更多的目的蛋白。 另一個優(yōu)點是排除了雜質(zhì)成分潛在的交叉反應(yīng)。請參考我們的亞細胞結(jié)構(gòu)分離技術(shù)方案。
Nonidet – P40(NP40)緩沖液
這是研究細胞質(zhì)蛋白、膜結(jié)合蛋白或者全細胞抽提物等常用的一種緩沖液。如果目標蛋白不能完全從不溶性或凝集物中提取,RIPA 緩沖液將 會更合適,它包含的離子型去污劑能更好溶解蛋白。
RIPA緩沖液(放射免疫沉淀分析緩沖液)
這種緩沖液對全細胞提取物和膜結(jié)合蛋白都非常有用,對提取細胞核蛋白來說,這種緩沖液比只含有 NP40 或 Triton X-100 的緩沖液更受歡 迎。但它會破壞蛋白與蛋白之間的相互作用,因此這在免疫沉淀測定中會有些問題。
在需要保存蛋白與蛋白相互作用,或者將蛋白變性降到最低(例如,抗體只能識別一個非變性表位)時,應(yīng)該使用不含離子型去污劑(SDS)的緩沖液和不含非離子型去污劑(Triton X-100)的緩沖液。用不含去污劑的裂解液,一般需配合機械剪切來裂解細胞,常用的 Dounce 均漿器 或者將細胞反復(fù)通過注射器針頭。這時簡單的Tris緩沖液就足夠了,但是對于膜結(jié)合蛋白或細胞骨架蛋白則需要含有去污劑的緩沖液。
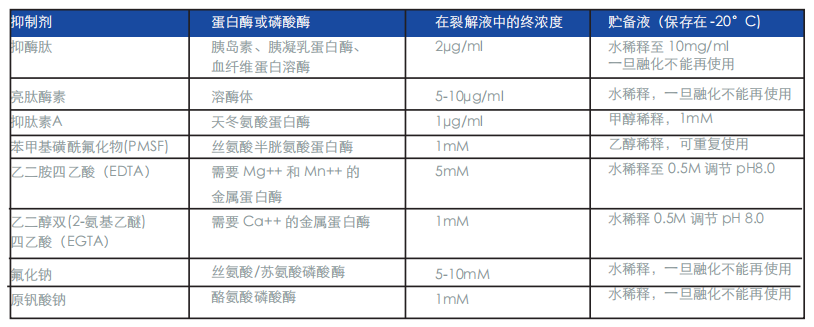
蛋白酶和磷酸酶抑制劑
一旦裂解發(fā)生,水解、去磷酸化和變性就開始了。如果樣本在冰上或始終在 4°C 存放以及一開始就往裂解液中加入適當抑制劑的話,這些反應(yīng)將可以大大減緩。混合(“雞尾酒”)的蛋白酶和磷酸酶抑制劑已經(jīng)商品化,也可以自己研制抑制劑的配比。
原釩酸鹽準備
所有步驟均在通風櫥中進行。
1.用雙蒸水溶解原釩酸鈉至 100mM。
2.用鹽酸調(diào) pH 值至 9.0。
3.加熱至無色。為盡量減少由于蒸發(fā)所致體積減小,加熱時加蓋。
4.冷卻至室溫。
5.調(diào) pH 值至 9.0。
6.再次加熱至無色。
7.再次加熱冷卻重復(fù)以上循環(huán)直至加熱冷卻后溶液 pH 值保持在 9.0。
8.用水補至起始體積。
8.-20°C 分裝保存,若變黃則廢棄。
細胞培養(yǎng)裂解物的制備
1.將細胞培養(yǎng)皿放置冰上并用冰冷的 PBS 洗滌細胞。
2.吸干 PBS 后,再加入冰冷的裂解液(每 107 細胞 / 100mm2 培養(yǎng)皿/150cm2 培養(yǎng)瓶加 1ml,每5x106 細胞 / 60mm2 培養(yǎng)皿/ 75cm2 培養(yǎng)瓶 加 0.5ml)。
3.用預(yù)冷的塑料細胞刮刀將貼壁細胞從培養(yǎng)皿上刮下,然后輕輕將細胞懸液轉(zhuǎn)移到預(yù)冷的小離心管中。
4.4°C 持續(xù)振蕩 30 分鐘。
5.4°C 預(yù)冷微型離心機中 16,000 x g 離心 20 分鐘。
6.從離心機中輕輕地取出離心管放置在冰上。將上清液吸出轉(zhuǎn)移到預(yù)冷的新管(放在冰上)中,棄沉淀。
組織裂解物的制備
1.用干凈器械解剖所需的組織,最好在冰上,并快速操作以防止蛋白酶降解。
2.將組織放入圓底離心管或 Eppendorf 管中,浸入液氮中“速凍”。樣本在 -80°C 儲存?zhèn)湟院笫褂没蚍旁诒狭⒓磩驖{。對于約 5mg 組織,向管中迅速加入約 300μl 裂解液并用電動勻漿器均漿,裂解液沖洗刀片兩次,每次 300μl,然后 4°C 持續(xù)振蕩 2 小時(將 回旋振蕩器放入冰箱)。裂解液的體積根據(jù)組織總量來決定。蛋白提取物不宜過于稀釋,以避免蛋白質(zhì)損失,并盡量減少樣品體積以便凝 膠上樣。最小濃度為 0.1mg/ml;最佳濃度為 1-5mg/ml。
3.微型離心機 4℃ 16,000rpm 離心 20 分鐘。從離心機中輕輕地取出離心管放置在冰上。吸出上清液放入預(yù)冷的新管(放在冰上)中,棄沉淀。
二、蛋白質(zhì)濃度的測定
用 Bradford、Lowry 或 BCA 方法測定蛋白質(zhì)含量,牛血清白蛋白是常用的蛋白標準。
一旦確定了每管的蛋白濃度就可以在 -20°C 或 -80°C 冷凍樣品備用,或為免疫沉淀反應(yīng)或凝膠上樣做準備。
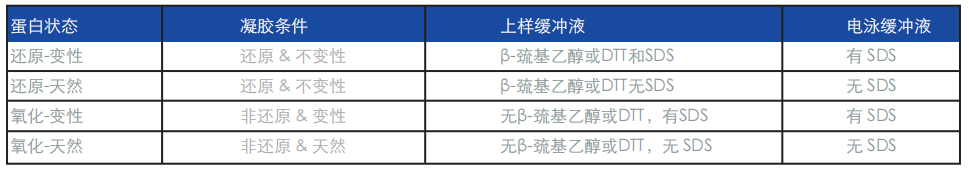
凝膠上樣:變性的和天然的,還原的和非還原的
1.a) 變性、還原樣品
抗體特異性識別目標蛋白的部位(即抗原表位)可能存在于蛋白的三維構(gòu)型內(nèi)部。為了能使抗體接近抗原表位,必須將蛋白的三維構(gòu)型打開, 即使蛋白變性。
要使蛋白質(zhì)變性,使用含陰離子變性去污劑十二烷基硫酸鈉 (SDS) 的上樣緩沖液,95-100°C 煮沸 5 分鐘,或者在 70°C 加熱5-10 分鐘,尤 其是研究跨膜蛋白時,因為煮沸更易聚集,聚集物不能有效的進入膠中。
標準品上樣緩沖液叫做2倍Laemmli緩沖液,最初描述在《自然》雜志上(1970 Aug 15;227(5259):680-5.)。也可以用4倍和6倍的樣品緩沖 液,可以減少緩沖液對樣品的稀釋。2 倍的樣品緩沖液和樣品以 1:1 的比例混合。
使用 SDS,通過 SDS 陰離子的粘附作用,所有的蛋白質(zhì)都帶負電荷,SDS 通過“纏繞”多肽鏈使蛋白變性。SDS 以 1.4:1 的比例結(jié)合到蛋白 上,SDS 賦予多肽的負電荷數(shù)與蛋白的長度成比例,即變性的多肽成為負電荷云的“棒”,每一單位長度的多肽帶有相同的電荷數(shù)或電荷云密度。
在變性 SDS-PAGE 中,遷移率不是由多肽固有的電荷數(shù)目來決定,而是由多肽的分子量來決定。SDS 的純度尤為重要,蛋白質(zhì)被染色的背 景與蛋白條帶能顯示出 SDS 質(zhì)量的好壞。
通過加入β巰基乙醇或二硫蘇糖醇(DTT),按照分子量大小進行分離,在蛋白形成自由彎曲之前減少二硫鍵的形成是非常必要的。上樣緩沖液中加入甘油能增加樣品的密度,使樣品停留在樣品池的底部,防止外溢和使凝膠上樣不規(guī)則。
為了能看到蛋白的遷移,通常在上樣緩沖液中加入小分子的離子型染料(如溴酚藍)。染料在混合物中的遷移速度最快,能夠提供一個遷移 前沿來監(jiān)測分離的過程。
蛋白質(zhì)樣品處理時,加熱前后都要用漩渦振蕩器徹底混勻樣品,使溶解徹底。
2.b) 天然的未降解樣品
有些抗體識別的抗原表位在抗原的天然構(gòu)型中由非臨近氨基酸組成。雖然這些氨基酸在原始序列中是彼此分開的,但它們在蛋白的三維結(jié)構(gòu) 中是相互靠近的。抗體只能辨認在折疊結(jié)構(gòu)表面上的抗原。
在這樣的情況下進行非變性條件 WB 是不可避免的,這一點會在產(chǎn)品的數(shù)據(jù)表上的應(yīng)用部分提到。總之,非變性條件就意味著樣品和電泳緩 沖液中不加入 SDS,以及不加熱樣品。
有些抗體僅僅識別非還原形式的蛋白質(zhì),如氧化形式(特別是半胱氨酸殘基)的蛋白質(zhì)。引起降解的試劑β巰基乙醇和 DTT 必須從上樣緩沖 液和電泳緩沖液中除去。
上一篇:熒光染色
下一篇:蛋白質(zhì)印跡—電泳

微信掃碼在線客服