TECHNICAL COLUMN
學(xué)習(xí)資源當(dāng)前位置:首頁(yè) > 學(xué)習(xí)資源
近年來(lái),開(kāi)發(fā)蛋白靶向降解技術(shù)成為藥物研發(fā)新的熱門(mén)方向。蛋白降解技術(shù)的研究使得許多已知的不可成藥靶點(diǎn)成為可成藥靶點(diǎn),并有望克服耐藥性問(wèn)題。蛋白靶向降解技術(shù)的研究主要是用于去除特定腫瘤蛋白,在自身免疫疾病等治療方面的研究也取得了較大的突破。
如何通過(guò)作用于絕大多數(shù)的不可成藥靶點(diǎn)來(lái)開(kāi)發(fā)藥物成為許多公司的研發(fā)重點(diǎn),當(dāng)前研究最多的是利用核酸藥物或基因治療的手段,對(duì)這些靶點(diǎn)的基因水平進(jìn)行控制,以達(dá)到控制靶點(diǎn)蛋白水平的目的。
細(xì)胞內(nèi)蛋白降解途徑主要有溶酶體途徑和泛素-蛋白酶體系統(tǒng)(ubiquitin - proteasome system , UPS)。其中,泛素-蛋白酶體系統(tǒng)是體內(nèi)蛋白降解的主要途徑,體內(nèi)80%的蛋白通過(guò)該途徑降解。因此,蛋白降解技術(shù)相關(guān)的研究也主要圍繞此途徑開(kāi)展,相關(guān)項(xiàng)目進(jìn)展也更快。
蛋白靶向降解(TPD)技術(shù)不僅可以靶向傳統(tǒng)意義上不可成藥的蛋白,而且相比于蛋白活性抑制劑可以更為徹底地阻斷靶蛋白的生物功能,是近年來(lái)藥物研發(fā)的熱點(diǎn)。目前TPD蛋白降解劑主要依賴(lài)泛素-蛋白酶體(如蛋白水解靶向嵌合體PROTACs)或者溶酶體(如溶酶體靶向嵌合體LYTACs),而這兩者是真核細(xì)胞有膜細(xì)胞器(如線粒體、葉綠體、過(guò)氧化物酶體等)內(nèi)所不具備的。因此目前已有的蛋白靶向降解技術(shù)對(duì)于有膜細(xì)胞器內(nèi)特定蛋白的降解無(wú)能為力。近日,中科院杭州醫(yī)學(xué)所的方曉紅團(tuán)隊(duì)利用線粒體基質(zhì)中豐富的AAA+蛋白水解酶,發(fā)展了一種具有普適性、可模塊化設(shè)計(jì)的線粒體基質(zhì)蛋白靶向降解新方法。
線粒體被稱(chēng)為細(xì)胞的能量工廠,至今已在線粒體中發(fā)現(xiàn)1000多種蛋白質(zhì),廣泛參與細(xì)胞的生長(zhǎng)、運(yùn)動(dòng)、應(yīng)激響應(yīng)等生物學(xué)過(guò)程。線粒體蛋白的異常是諸如神經(jīng)退行性疾病、腫瘤等惡性疾病的重要驅(qū)動(dòng)因素。靶向調(diào)控線粒體基質(zhì)蛋白的穩(wěn)定性及降解在疾病治療和藥物開(kāi)發(fā)中具有重要價(jià)值。雖然線粒體基質(zhì)不具有泛素-蛋白酶體或者溶酶體,但是富集了多種由細(xì)胞核基因編碼的AAA+蛋白酶(如ClpP、LONP1等)。線粒體內(nèi)部主要通過(guò)這些AAA+蛋白酶對(duì)靶蛋白進(jìn)行水解切割,以精確控制線粒體的蛋白穩(wěn)態(tài)。同時(shí)在細(xì)胞應(yīng)激狀態(tài)下,胞漿中大量變性蛋白質(zhì)被也會(huì)被轉(zhuǎn)運(yùn)到線粒體基質(zhì)中,經(jīng)由AAA+蛋白酶進(jìn)行快速降解。以上特性提示可利用這一類(lèi)AAA+蛋白酶發(fā)展線粒體基質(zhì)蛋白適用的靶向降解技術(shù)。
在針對(duì)腫瘤標(biāo)志物的前期研究中,科技部納米重大科學(xué)研究計(jì)劃項(xiàng)目首席科學(xué)家(2007-2017)方曉紅教授團(tuán)隊(duì),在針對(duì)腫瘤標(biāo)志物的前期研究中,通過(guò)發(fā)展核酸適體技術(shù)、高通量蛋白抑制劑篩選技術(shù)等,發(fā)現(xiàn)可以通過(guò)小分子化合物誘導(dǎo)線粒體基質(zhì)蛋白經(jīng)由AAA+蛋白酶快速降解,證明了利用AAA+蛋白酶來(lái)靶向降解線粒體基質(zhì)蛋白的可行性(J. Am. Chem. Soc., 2019, 141, 18492-18499)。然而上述線粒體基質(zhì)蛋白小分子降解劑需要針對(duì)不同蛋白進(jìn)行個(gè)性化的高通量篩選才能獲得,開(kāi)發(fā)更為普適性的、可模塊化設(shè)計(jì)的線粒體基質(zhì)蛋白降解新方法具有重要意義。
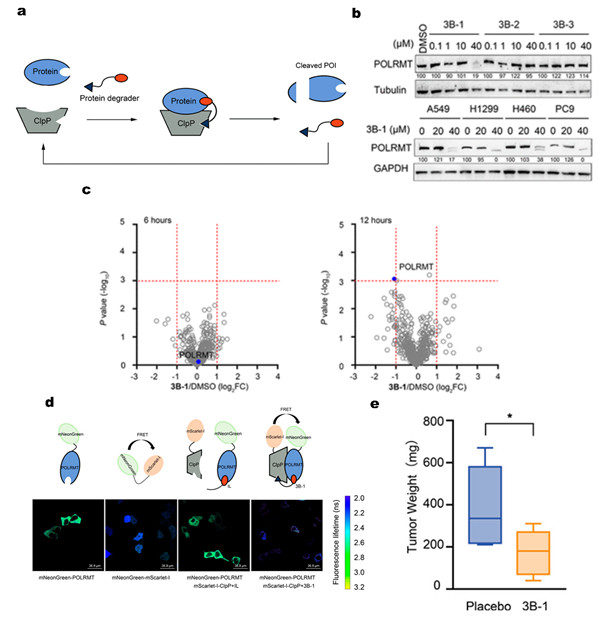
研究團(tuán)隊(duì)借鑒經(jīng)典的PROTAC分子結(jié)構(gòu),設(shè)計(jì)了能夠誘導(dǎo)線粒體基質(zhì)靶蛋白與AAA+蛋白酶相互作用并高效水解的線粒體蛋白酶靶向嵌合體MtPTAC。以AAA+蛋白酶中水解能力最強(qiáng)的ClpP為蛋白降解機(jī)器,以定位于線粒體內(nèi)并具有促進(jìn)腫瘤生長(zhǎng)功能的線粒體RNA聚合酶POLRMT為靶蛋白,合成了由聚乙二醇PEG鏈連接ClpP和POLRMT配體的MtPTAC分子。利用多種細(xì)胞系證實(shí)了設(shè)計(jì)合成的MtPTAC分子具備強(qiáng)大的線粒體基質(zhì)靶蛋白降解能力。進(jìn)一步表征分析了MtPTAC的濃度、時(shí)間以及PEG鏈長(zhǎng)對(duì)靶蛋白切割降解效率的影響。通過(guò)細(xì)胞FRET成像、分子動(dòng)力學(xué)模擬等探究了MtPTAC降解靶蛋白的分子機(jī)制,證實(shí)合理設(shè)計(jì)的MtPTAC分子可以拉近靶蛋白POLRMT與AAA+蛋白酶ClpP的空間距離,并觸發(fā)ClpP依賴(lài)性的POLRMT水解。高通量蛋白組學(xué)實(shí)驗(yàn)結(jié)果表明這種水解具有較好的特異性,對(duì)線粒體其他蛋白的表達(dá)量影響小。最后通過(guò)體外細(xì)胞實(shí)驗(yàn)與小鼠體內(nèi)成瘤實(shí)驗(yàn),證實(shí)MtPTAC分子在體內(nèi)可通過(guò)對(duì)靶蛋白的切割降解展示出比單獨(dú)使用靶蛋白活性抑制劑更強(qiáng)的抗腫瘤能力。
線粒體基質(zhì)蛋白靶向降解MtPTAC技術(shù)為線粒體相關(guān)疾病的治療提供了新思路。值得注意的是,過(guò)去報(bào)道的蛋白降解劑只是拉近了靶蛋白與蛋白降解器之間的空間距離,而MtPTAC中使用的AAA+蛋白酶結(jié)合配體還可直接增強(qiáng)其水解酶活性,是首個(gè)結(jié)合-激活型小分子降解劑。綜上,該工作發(fā)展了一種新的細(xì)胞器靶蛋白降解技術(shù),為T(mén)PD提供了一個(gè)新的平臺(tái)策略。
上述研究工作近期發(fā)表于J. Am. Chem. Soc.上,第一作者為中科院杭州醫(yī)學(xué)所博士生王大馳(與中國(guó)科學(xué)技術(shù)大學(xué)聯(lián)合培養(yǎng))和博士后王文溪,通訊作者為中科院杭州醫(yī)學(xué)所單分子生物醫(yī)學(xué)研究團(tuán)隊(duì)的方曉紅研究員和周衛(wèi)副研究員。本工作得到了國(guó)家重點(diǎn)研發(fā)計(jì)劃、國(guó)家自然科學(xué)基金委以及浙江省自然科學(xué)基金項(xiàng)目的資助。
文獻(xiàn)參考:
Mitochondrial Protease Targeting Chimeras for Mitochondrial Matrix Protein Degradation
Dachi Wang, Wenxi Wang, Le Fang, Lubin Qi, Yuchao Zhang, Jie Liu, Yuxin Liang, Hongwei Yang, Mengjie Wang, Xiaojian Wei, Ruibin Jiang, Yuan Liu, Wei Zhou*, and Xiaohong Fang*
J. Am. Chem. Soc., 2023, DOI: 10.1021/jacs.3c03756

微信掃碼在線客服