PRODUCT CENTER
特色產(chǎn)品當前位置:首頁 > 特色產(chǎn)品
基因治療,特別是基于腺相關病毒(AAV)載體的基因治療,已被證明在多種遺傳性疾病的治療中具有巨大潛力。AAV載體因其低免疫原性、長期表達穩(wěn)定性和廣泛的宿主范圍而被廣泛應用于臨床前和臨床試驗中。然而,實現(xiàn)高效、低成本的AAV載體大規(guī)模純化仍是當前面臨的一大挑戰(zhàn)。傳統(tǒng)的純化方法如離子交換層析和親和層析雖能有效去除宿主細胞蛋白(HCPs),但在分離全基因組AAV載體與空殼或中間態(tài)粒子方面效果有限。
現(xiàn)有純化方法的局限性
現(xiàn)有純化方法存在幾個顯著問題:
小規(guī)模和低效性:傳統(tǒng)方法如CsCl密度梯度離心通常耗時較長(通常需要兩天),且處理量有限。
免疫原性和安全性:空殼AAV載體可能降低轉(zhuǎn)導效率并引發(fā)不必要的免疫反應,同時其內(nèi)的雙鏈RNA(dsRNA)可能激活先天免疫反應。
臨床適用性:碘克沙醇因交叉反應而不適用于碘過敏患者。

近期《Large-scale purification of functional AAV particles packaging the full genome using short-term ultracentrifugation with a zonal rotor》文章帶來了新的進展。文章研究旨在開發(fā)一種基于兩步CsCl密度梯度超速離心的大規(guī)模、短期純化方法,用于從培養(yǎng)上清液中高效分離功能性全基因組AAV載體顆粒。
研究方法
AAV載體制備
使用表達腺病毒E1a、E1b和Bcl-xL的293EB細胞系,在大型生物反應器中培養(yǎng)并轉(zhuǎn)染以產(chǎn)生AAV載體。轉(zhuǎn)染后收集培養(yǎng)上清液,經(jīng)核酸酶處理去除殘余DNA。
超速離心純化
使用帶有分區(qū)轉(zhuǎn)子的超速離心機,通過兩步CsCl密度梯度(25–27%和38–40%)進行超速離心,縮短離心時間至4–5小時。通過測量各離心管中溶液的折射率(RI)來確定分離后的AAV載體顆粒。
AAV載體評價
使用定量聚合酶鏈反應(qPCR)、Western blot和流式細胞術評估AAV載體的基因組拷貝數(shù)、衣殼蛋白含量和轉(zhuǎn)導效率。通過分析超速離心(AUC)和透射電子顯微鏡(TEM)分析AAV載體的純度和形態(tài)。使用ddPCR評估AAV載體包裝的基因組完整性和空殼AAV載體中可能存在的ITR片段。
AAV質(zhì)量控制J標準:
Progen品牌的anti-AAV VP1/VP2/VP3 mouse antibody,貨號:65158
可檢測:AAV1, AAV2, AAV3, AAV5, AAV6, AAV7, AAV8, AAV9, AAVDJ, AAVrh10
在本研究中,Progen品牌的anti-AAV VP1/VP2/VP3 mouse antibody在Western blot分析中發(fā)揮了關鍵作用,具體體現(xiàn)在以下幾個方面:
AAV衣殼蛋白檢測
該抗體能夠特異性識別AAV衣殼蛋白VP1、VP2和VP3,這些蛋白是AAV顆粒的結構組成部分,對于AAV的完整性和功能性至關重要。通過Western blot,研究人員能夠直觀地檢測到不同離心分數(shù)中AAV衣殼蛋白的存在與否,進而判斷AAV載體的純度和完整性。
純化效果的驗證
在AAV載體純化過程中,準確評估純化效果是確保最終產(chǎn)品質(zhì)量的關鍵。通過檢測AAV衣殼蛋白,可以驗證超速離心純化方法是否有效去除了雜質(zhì)(如宿主細胞蛋白和空殼AAV載體),同時保留了功能性全基因組AAV載體。
質(zhì)量控制
在AAV載體的生產(chǎn)和純化過程中,質(zhì)量控制是確保產(chǎn)品安全性和有效性的重要環(huán)節(jié)。anti-AAV VP1/VP2/VP3 mouse antibody作為一種高質(zhì)量的質(zhì)量控制工具,能夠幫助研究人員實時監(jiān)測AAV載體的純化進度和質(zhì)量,確保產(chǎn)品符合臨床應用的標準。
實驗結果
高效分離全基因組AAV載體
通過兩步CsCl密度梯度超速離心,成功實現(xiàn)了從大量培養(yǎng)上清液中高效分離全基因組AAV載體的目標。離心時間縮短至4–5小時,且處理量提升至1000mL。
高純度AAV載體
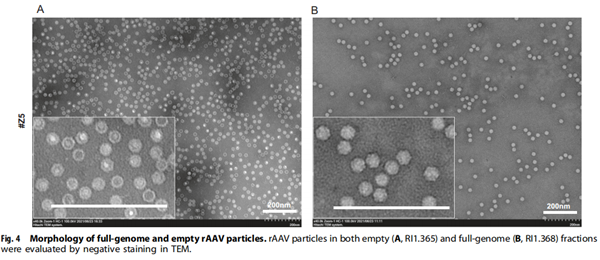
AUC和TEM分析表明,純化后的AAV載體具有高純度,空殼和中間態(tài)粒子得到有效去除。ddPCR分析進一步證實,空殼AAV載體中含有ITR片段,但全基因組AAV載體則包含完整的基因組序列。
功能性驗證
轉(zhuǎn)導效率實驗表明,純化后的AAV載體在目標細胞中具有高轉(zhuǎn)導效率,進一步驗證了其功能性。
結論
本研究開發(fā)了一種基于兩步CsCl密度梯度超速離心的大規(guī)模、短期純化方法,用于從培養(yǎng)上清液中高效分離高純度全基因組AAV載體。該方法不僅縮短了離心時間并提高了處理量,而且通過一系列評估手段驗證了純化后AAV載體的高純度和功能性。特別是,Progen品牌的anti-AAV VP1/VP2/VP3 mouse antibody在Western blot分析中的成功應用,為AAV載體的質(zhì)量控制提供了有力支持。未來,該純化方法有望在臨床研究和GMP生產(chǎn)中發(fā)揮重要作用。
更多AAV整體研究方案,歡迎垂詢中國區(qū)總代理,艾美捷科技!索取下方手冊資料


微信掃碼在線客服