PRODUCT CENTER
特色產(chǎn)品當(dāng)前位置:首頁(yè) > 特色產(chǎn)品
PNGase F,也稱為肽N-糖苷酶F,是一種在分子生物學(xué)和生物化學(xué)研究中常用的酶。它在研究糖蛋白方面發(fā)揮著重要作用,糖蛋白是附著有糖分子(糖鏈)的蛋白質(zhì)。PNGase F用于從糖蛋白中移除N-連接的糖鏈,使其成為各種科學(xué)應(yīng)用中的重要工具。
PNGase F的使用:
糖蛋白去糖基化:PNGase F酶促地從糖蛋白中切割N-連接的糖鏈。N-連接的糖鏈?zhǔn)且环N特定類型的糖鏈,它附著在蛋白質(zhì)氨基酸序列中的天冬酰胺(N)殘基上。
在糖蛋白分析中的重要性:從糖蛋白中移除糖鏈對(duì)于研究其底層蛋白質(zhì)結(jié)構(gòu)和功能至關(guān)重要。它允許研究人員分析蛋白質(zhì)核心,準(zhǔn)確確定其分子量,并研究其生物活性。
應(yīng)用:PNGase F在各種應(yīng)用中廣泛使用,包括蛋白質(zhì)組學(xué)、結(jié)構(gòu)生物學(xué)、免疫學(xué)和藥物研究。它在表征糖蛋白、理解它們?cè)诩?xì)胞過程中的作用以及開發(fā)治療藥物方面發(fā)揮著重要作用。
生物醫(yī)學(xué)研究:在生物醫(yī)學(xué)研究中,PNGase F用于分析與癌癥、糖尿病和傳染病等疾病相關(guān)的糖蛋白。它有助于識(shí)別生物標(biāo)志物和潛在的藥物靶標(biāo)。
質(zhì)量控制:在生物制藥行業(yè)中,PNGase F被用來(lái)確保基于糖蛋白的藥物(如單克隆抗體)的質(zhì)量和一致性,通過驗(yàn)證糖鏈結(jié)構(gòu)和監(jiān)測(cè)糖基化模式。
糖蛋白工程:研究人員可以使用PNGase F對(duì)糖蛋白進(jìn)行特定目的的修改,例如提高藥物效果或改變糖鏈結(jié)構(gòu),用于研究或治療應(yīng)用。
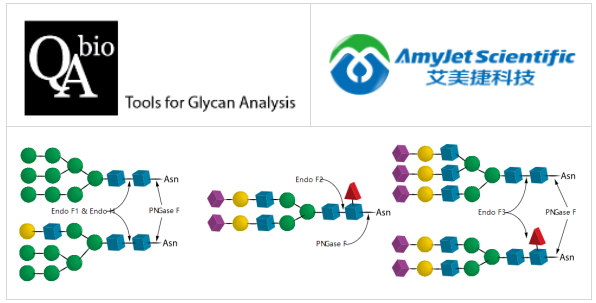
Endo F1、Endo F2、Endo F3、Endo H和PNgase F的活性比較
艾美捷QA-Bio-PNGase F內(nèi)容:
PNGase F 在 20 mM Tris-HCl,pH 7.5
隨附20 uL 和 60 uL 包裝大小:
5倍反應(yīng)緩沖液 7.5 – 250 mM 磷酸鈉,pH 7.5
變性溶液 – 2% SDS,1 M β-巰基乙醇
Triton X-100 – 15% 溶液
比活性 >25 U/mg
活性 5 U/ml
分子量 35,000 道爾頓
pH 范圍 6-10,Z佳 pH 7.5
QA-Bio-PNGase F 協(xié)議:
向 Eppendorf 管中添加最多 200 ?g 的糖蛋白。用去離子水調(diào)整至 35 ?l 的最終體積。
添加 10 ?l 的 5倍反應(yīng)緩沖液 7.5 和 2.5 ?l 的變性溶液。在 100°C 下加熱 5 分鐘。
冷卻。添加 2.5 ul 的 Triton X-100 并混合。
向反應(yīng)中添加 2.0 ul 的酶。在 37°C 下孵育 3 小時(shí)。
特異性 切割所有天冬酰胺連接的復(fù)雜型、混合型或高甘露糖寡糖,除非是α(1-3)核心巖藻糖化的;天冬酰胺必須在兩端都有肽鍵,無(wú)Endo F
比活性 定義為在 37°C,pH 7.5 的條件下,每分鐘催化 1 微摩爾變性的牛胰核糖核酸酶 B 釋放 N-連接寡糖所需的酶量。通過 SDS-PAGE 監(jiān)測(cè)切割(切割后的牛胰核糖核酸酶 B 遷移更快)。
QA-Bio-PNGase F文獻(xiàn)參考:
Bayer, E.A., F. De Meester, T. Kulik and M. Wilchek. Preparation of deglycosylated egg white avidin. Appl Biochem Biotech 53: 1-9 (1995)
Elder, J.H. and S. Alexander. Endo-b-N-Acetylglucosaminidase F: endoglycosidase from Flavobacterium meningosepticum that cleaves both high-mannose and complex glycoproteins. Proc Natl Acad Sci USA 79: 4540-4544 (1982)
Tarentino, A .L., C.M. Gomez and T.H. Plummer, Jr. Deglycosylation of asparagine-linked glycans by peptide :N-glycosidase F. Biochemistry 24: 4665-4671 (1985)
Tarentino A.L. and T.H. Plummer. Enzymatic deglycosylation of asparagine -linked glycans: purification, properties, and specificity of oligosaccharide-cleaving enzymes from Flavobacterium meningosepticum. Meth Enzymol 230: 44-57 (1994)
Trimble R.B. and A.L. Tarentino. Identification of distinct endoglycosidase (endo) activities in Flavobacterium meningosepticum: endo F1 , endo F2 and endo F3. Endo F1 and endo H hydrolyze only high mannose and hybrid glycans. J Biol Chem 266: 1646-1 651 (1991)
Taga, E. M., A. Waheed and R. L. Van Etten. Structural and chemical characterization of a homogeneous peptide-N-glycosidase from almond. Biochemistry 23: 815-22 (1984)
Tarentino AL, Trimble RB, Plummer TH. Enzymatic approaches for studying the structure, synthesis, and processing of glycoproteins. Methods in Cell Biology: 32: 111–39 (1989)
Anthony L. , Tarentino and Thomas H. Plummer Jr. Enzymatic deglycosylation of asparagine-linked glycans: Purification, properties, and specificity of oligosaccharide-cleaving enzymes from Flavobacterium meningosepticum. Methods in Enzymology: 230: 44-57. (1994)
Tarentino AL, Plummer TH. Oligosaccharide accessibility to peptide:N-glycosidase as promoted by protein-unfolding reagents. The Journal of Biological Chemistry. 257 (18): 10776–80. (1982)
艾美捷科技是QA-Bio的中國(guó)代理商,為科研工作者提供優(yōu)質(zhì)的產(chǎn)品與服務(wù)。

微信掃碼在線客服