TECHNICAL COLUMN
學(xué)習(xí)資源當(dāng)前位置:首頁 > 學(xué)習(xí)資源
2024年2月1日,同濟大學(xué)醫(yī)學(xué)院王平課題組在Nature在線發(fā)表題為“7-Dehydrocholesterol dictates ferroptosis sensitivity”的最新論文,研究發(fā)現(xiàn)遠端膽固醇合成途徑中產(chǎn)生的中間甾醇7-DHC是一種新的鐵死亡內(nèi)源抑制因子,闡明了7-DHC依賴其5,7-不飽和雙鍵的結(jié)構(gòu)特性直接抑制磷脂過氧化的具體機制,提示甾醇與磷脂的過氧化在鐵死亡過程中具有不同作用。
細胞程序性死亡(programmed cell death)是受到基因調(diào)控的有序的細胞死亡方式,其對生命體的發(fā)育、代謝、微環(huán)境穩(wěn)態(tài)維持和疾病發(fā)生等過程至關(guān)重要,主要包括凋亡、程序性壞死和焦亡等形式。鐵死亡是近年來鑒定的一種由鐵依賴的磷脂過氧化引起的新型程序性細胞死亡形式,與細胞中多種代謝進程,如氨基酸代謝、鐵代謝、磷脂代謝、輔酶Q10、谷胱甘肽合成等息息相關(guān),并在腫瘤、器官缺血再灌注損傷和神經(jīng)退行性疾病等多種疾病中發(fā)揮重要作用。解析鐵死亡發(fā)生機制是細胞程序性死亡領(lǐng)域的前沿重大科學(xué)問題,并為治療上述疾病帶來了新的靶向策略。
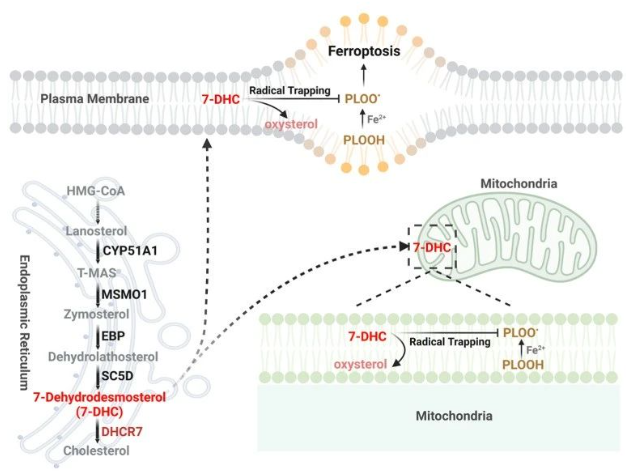
為了全面探究鐵死亡的調(diào)控機制,王平教授團隊首先通過全基因組CRISPR篩選技術(shù),發(fā)現(xiàn)遠端膽固醇合成通路關(guān)鍵酶能夠差異調(diào)控鐵死亡敏感性,他們通過內(nèi)源敲除關(guān)鍵基因及外源回補不同中間代謝物等實驗確定了遠端膽固醇合成通路中的中間代謝物甾醇—7-脫氫膽固醇(7- Dehydrocholesterol)的水平直接影響細胞對鐵死亡的敏感性。研究團隊進一步對機制進行解析,通過FENIX等實驗體系以及中間代謝物結(jié)構(gòu)特征的對比,發(fā)現(xiàn)7-DHC依賴其B環(huán)中的5,7不飽和雙鍵,以自身的氧化為代價直接抑制磷脂過氧化的發(fā)生,從而抑制鐵死亡。有趣的是,他們發(fā)現(xiàn)麥角固醇(真菌中的主要甾醇形式)在B環(huán)中也存在5,7-不飽和雙鍵,同樣能夠抑制磷脂過氧化及鐵死亡的發(fā)生,提示這一類5,7-不飽和甾醇在抑制磷脂過氧化的功能上具有一定的普適性及保守性。
鐵死亡參與癌癥和器官缺血再灌注損傷疾病的發(fā)生發(fā)展,但在兩種疾病中發(fā)揮著不同的功能。其中,誘導(dǎo)腫瘤細胞發(fā)生鐵死亡能夠作為癌癥治療的策略,而抑制機體細胞的鐵死亡則可以作為保護器官損傷的策略。因此,通過靶向抑制遠端膽固醇合成中關(guān)鍵酶來調(diào)控內(nèi)源7-DHC的水平,可能成為臨床治療腫瘤或器官損傷的新靶標。在腫瘤治療方面,作者首先通過對CRISPR篩選數(shù)據(jù)庫分析發(fā)現(xiàn),一些腫瘤細胞系的生存很可能依賴于7-DHC。進一步實驗證明,抑制SU-DHL-8細胞中7-DHC的產(chǎn)生能夠直接誘導(dǎo)鐵死亡的發(fā)生,而小鼠水平的成瘤實驗也證明靶向抑制7-DHC的產(chǎn)生能夠在體誘導(dǎo)腫瘤細胞鐵死亡并抑制腫瘤的生長。另一方面,通過藥理學(xué)靶向抑制DHCR7可以有效在體積累7-DHC并治療小鼠缺血再灌注腎損傷。
為代謝穩(wěn)態(tài)維持與細胞命運決定之間的調(diào)控機制提供了新的理論依據(jù),也為治療腫瘤及缺血再灌注器官損傷等鐵死亡密切相關(guān)疾病提供了潛在的靶點和策略。
文章來源:
Yaxu Li, Qiao Ran, Qiuhui Duan, Jiali Jin et al,7-Dehydrocholesterol dictates ferroptosis sensitivity.https://doi.org/10.1038/s41586-023-06983-9.

微信掃碼在線客服