TECHNICAL COLUMN
學(xué)習(xí)資源當(dāng)前位置:首頁(yè) > 學(xué)習(xí)資源
免疫組織化學(xué) (IHC) 是確定組織切片上蛋白的存在與否及存在位置的一種方法。盡管這種方法在定量分析時(shí)靈敏度較免疫印跡法或 ELISA 等 免疫測(cè)定方法低,但是它能觀察到整個(gè)組織的情況。適用于評(píng)估癌癥等疾病的發(fā)展及治療情況。因此,從 IHC 獲得的信息結(jié)合顯微技術(shù)提供 了一副“宏圖”,使來(lái)自其它方法的數(shù)據(jù)有據(jù)可依。
免疫組織化學(xué)染色是抗體識(shí)別靶抗原的過(guò)程。因?yàn)榭贵w是高度特異的,因此它只與組織切片上相應(yīng)的蛋白結(jié)合。應(yīng)用顯色檢測(cè)法即能看到抗 原-抗體反應(yīng),一種顯色方法是將與酶結(jié)合的抗體作為底物在蛋白位點(diǎn)產(chǎn)生一種色素沉著,另外一種方法是熒光檢測(cè)法,即將熒光染料結(jié)合到 抗體上,應(yīng)用熒光顯微技術(shù)檢測(cè)。
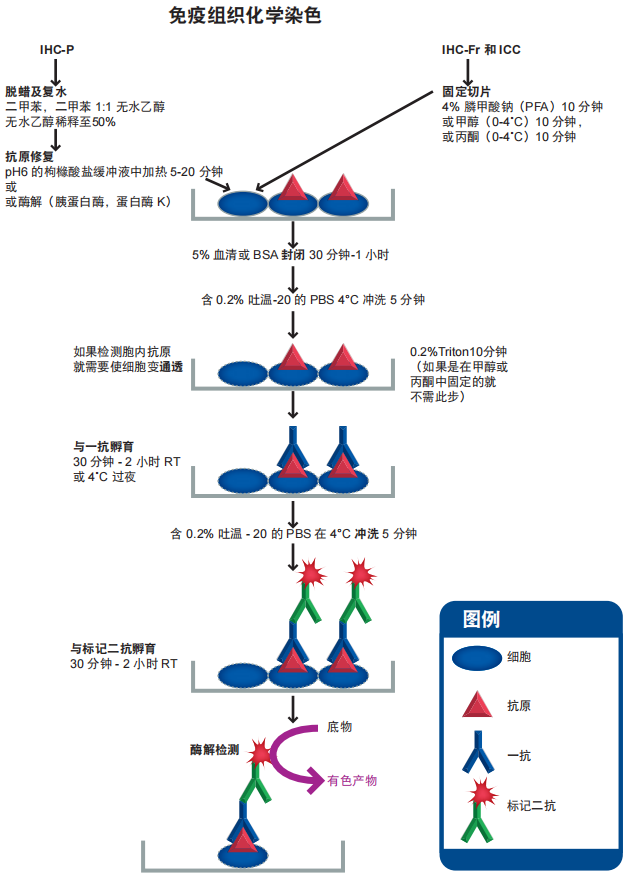
IHC-P 涉及到固定(通常在中性甲醛溶液中固定)組織的染色,然后是在切割之前的石蠟包埋。下面是 IHC-P 技術(shù)的基本步驟:
1.組織的固定和包埋
2.切割并封固切片
3.脫蠟復(fù)水
4.抗原修復(fù)
5.免疫組織化學(xué)染色
6.復(fù)染(如果需要)
7.脫水并用封固劑封固
8.顯微鏡下觀察染色
目錄
優(yōu)化 IHC-P 新抗體
1.抗原修復(fù)
2.一抗?jié)舛?/p>
3.檢測(cè)
固定
脫蠟
抗原修復(fù)
1.熱誘導(dǎo)抗原表位修復(fù)的緩沖溶液
2.熱誘導(dǎo)抗原表位修復(fù)方法
3.具有酶活性抗原的修復(fù)
免疫組織化學(xué)染色和檢測(cè)實(shí)驗(yàn)方案
1.一般指南
2.手冊(cè)
3.對(duì)照
4.信號(hào)放大
相關(guān)資料
優(yōu)化 IHC-P 新抗體
一種新抗體要應(yīng)用到 IHC-P 中,就必須找到適宜這種抗體的染色條件。每種抗原都有一個(gè)最佳修復(fù)方法。每種抗體都有一個(gè)最佳稀釋濃度。
抗原修復(fù)
試著在沒(méi)有抗原修復(fù)和應(yīng)用下列抗原修復(fù)方法修復(fù)抗原的情況下染色,詳細(xì)操作見抗原修復(fù)部分(第 30 頁(yè))。
1.熱修復(fù):枸櫞酸鈉 10 mM,pH 6.0
2.熱修復(fù):Tris/EDTA pH 9.0
3.酶解:胰蛋白酶、胃蛋白酶或其它蛋白酶。
抗原修復(fù)的最佳方法確定后,就可以進(jìn)行最佳抗體濃度的確定了。
一抗?jié)舛?/strong>
如果抗體濃度未知,我們建議用 0.5 μg/ml 和 5 μg/ml 4°C 過(guò)夜。如果抗體未經(jīng)純化,我們建議開始時(shí)使用下面的初始稀釋度,也可以嘗試 20 倍的高倍稀釋度。
1.全抗血清:1/50
2.腹腔積液:1/100
3.組織培養(yǎng)上清:不稀釋(也指“neat”)
檢測(cè)
我們建議使用辣根過(guò)氧化物酶 (HRP),在光學(xué)顯微鏡下觀察。過(guò)氧化物/DAB 作為底物和色素原。熒光顯微鏡方法中有多種熒光
染料標(biāo)記的 抗體,具體用哪一種要根據(jù)試驗(yàn)需要來(lái)進(jìn)行選擇。
固定
正確的固定是免疫組織化學(xué)方法的關(guān)鍵。最常用的是 10% 中性甲醛溶液 (NBF)。Abcam 說(shuō)明書推薦 IHC-P 使用該固定劑,除非另有說(shuō)明。 其它不常用的固定劑如多聚甲醛 (PFA) 或 Bouin's 液(甲醛/苦味酸)等。這些固定劑的配方詳見緩沖液部分,第71頁(yè)。
理想的固定時(shí)間取決于組織塊的大小和類型。對(duì)于大多數(shù)組織來(lái)說(shuō),通常固定時(shí)間在 18-24 小時(shí)之間較為理想。固定不足會(huì)導(dǎo)致組織切片因 邊緣染色而信號(hào)強(qiáng),中間未染上而無(wú)信號(hào)。固定過(guò)度將會(huì)屏蔽抗原表位。抗原修復(fù)有助于克服屏蔽作用,但是如果固定時(shí)間太長(zhǎng)(比如一個(gè) 星期)那么抗原修復(fù)也無(wú)濟(jì)于事。
固定后,將組織塊包埋于石蠟中,用切片機(jī)切成理想厚度(依據(jù)組織一般大約在 5-20 微米),然后將切片附著在玻片上,封固最好用正電荷吸 附或 3-氨基-丙酯-三-乙氧基-硅烷 (APES),室溫過(guò)夜脫水并徹底干燥。如果切片不能很好的附著在玻片上,可以將其至于 60°C 放置數(shù)小時(shí)。
脫蠟
在開始染色之前,切片必須先脫蠟至水。脫蠟不徹底,就會(huì)使切片很難染上色。
材料及試劑
二甲苯
無(wú)水乙醇
95% 乙醇
方法
將切片置于架子上,依據(jù)下列方法沖洗:
1.二甲苯:2 X 3 分鐘
2.二甲苯與無(wú)水乙醇 1:1 混勻:3 分鐘
3.無(wú)水乙醇:2 X 3 分鐘
4.95% 乙醇:3 分鐘
5.70 %乙醇:3 分鐘
6.50 % 乙醇::3 分鐘
7.冷的自來(lái)水小水流沖洗
在開始抗原修復(fù)前確保切片一直浸沒(méi)在水中以防變干,否則特異抗體不易結(jié)合且會(huì)有很高的染色背景。
抗原修復(fù)
大多數(shù)甲醛固定的組織在開始染色之前都需要先修復(fù)抗原,這是由于在固定過(guò)程中產(chǎn)生了亞甲基橋使蛋白之間交聯(lián)屏蔽了抗原位點(diǎn)。兩種抗 原修復(fù)方法為熱修復(fù)法(稱之為熱誘導(dǎo)抗原表位修復(fù)或 HIER)和酶解法。
這些修復(fù)方法原理都是將亞甲基橋打斷,使抗原表位暴露出來(lái),以便于抗體結(jié)合。有的抗原適合酶解修復(fù),有的抗原適合熱修復(fù)。酶解修復(fù) 有時(shí)會(huì)損壞組織的形態(tài)結(jié)構(gòu),因此需要摸索酶濃度和作用時(shí)間。Tris/EDTA pH 9.0 的緩沖液適合于大多數(shù)抗原,pH 6.0 的枸櫞酸鈉緩沖液也 較為常用。以下網(wǎng)站解釋了為什么 Abcam 建議首選 Tris/EDTA pH 9.0 的緩沖液而不是 pH 6.0 的枸櫞酸鈉緩沖液。
熱抗原修復(fù)需要高壓鍋、微波爐或蒸煮鍋。另外,一些實(shí)驗(yàn)室將玻片置于修復(fù)溶液中 60°C 水浴過(guò)夜。除非抗原修復(fù)方法在抗體數(shù)據(jù)表中可 以找到,否則必須通過(guò)實(shí)驗(yàn)來(lái)確定適宜的修復(fù)。Abcam建議嘗試多種方法來(lái)確定適宜的修復(fù)方法,以便于獲得理想的染色。
1.熱修復(fù)緩沖溶液
下面是三種HIER較為常用的緩沖溶液,對(duì)于一個(gè)特定的抗體,在沒(méi)有其他研究者建議的情況下,要通過(guò)實(shí)驗(yàn)確定選用哪種修復(fù)緩沖液。
1.枸櫞酸鈉緩沖液 (10 mM Sodium Citrate, 0.05% 吐溫- 20, pH 6.0)
2.1 mM EDTA, 調(diào)至 pH 8.0
3.Tris/EDTA 緩沖液 (10mM Tris, 1 mM EDTA 溶液, 0.05% 吐溫-20, pH 9.0)
熱修復(fù)法
a) 高壓蒸汽法
玻片要置于金屬架上
材料及試劑
家用不銹鋼高壓鍋
加熱板
玻片架放置容器(容量大約 400-500ml)
抗原修復(fù)緩沖液(如 Tris/EDTA pH 9.0,枸櫞酸鈉 pH 6.0)
方法
1.將合適的抗原修復(fù)緩沖液加入高壓鍋內(nèi),然后將鍋置于加熱板并開至最大功率,此時(shí)不要把蓋子蓋緊。在等待煮沸過(guò)程中,按前面描述進(jìn) 行脫蠟至水。
2.煮沸后,將玻片從自來(lái)水中取出放入高壓鍋內(nèi)。小心熱溶液 - 使用鑷子。依照說(shuō)明書加上加壓閥。
3.高壓鍋達(dá)到最大壓力后(見操作手冊(cè)),維持 3 分鐘(見注意事項(xiàng) 1)。
4.3 分鐘過(guò)后,關(guān)掉加熱板,將高壓鍋取下放置。
5.打開高壓鍋閥門(見操作手冊(cè)),冷水冷卻鍋身。壓力降下后,打開鍋蓋,冷水冷卻 10 分鐘。小心熱溶液使用注意事項(xiàng)(見注意事項(xiàng) 2)。
6.參照手冊(cè)繼續(xù)染色。
注意事項(xiàng):
1.3 分鐘只是抗原修復(fù)的建議時(shí)間。低于 3 分鐘可能會(huì)使修復(fù)不徹底,導(dǎo)致染色較弱。而超過(guò) 3 分鐘可能會(huì)使修復(fù)過(guò)度,導(dǎo)致非特異性背景 染色,同時(shí)增加切片離解的幾率。因此需要做對(duì)照試驗(yàn),同樣的組織切片分別修復(fù) 1、2、3、4、5 分鐘后開始染色,針對(duì)所用的特異抗 體選擇最佳修復(fù)時(shí)間。
2.確保玻片徹底冷卻可以便于下一步操作,而且使抗原表位在經(jīng)歷高溫后復(fù)原。
b) 微波法
不建議使用家用微波爐。因?yàn)樗鼤?huì)導(dǎo)致抗原修復(fù)時(shí)冷熱不均。而且由于沒(méi)有高壓環(huán)境,修復(fù)時(shí)間較長(zhǎng),會(huì)使切片解離。建議使用科研專用微 波爐較為合適。大多品牌的科研專用微波爐都有加壓裝置,能持續(xù)保持 98°C 從而避免切片解離。唯一的缺陷就是它的價(jià)格昂貴。
使用該方法時(shí),修復(fù)緩沖液煮沸會(huì)大量蒸發(fā),要確保緩沖液的量,不能使切片變干。
玻片要置于塑料架子和塑料容器內(nèi),玻璃架和玻璃容器在加熱時(shí)會(huì)破裂。
材料和試劑
家用 (850W) 或科研專用微波爐
微波爐專用玻片放置架及容器(容量大約 400-500ml)或染色缸
抗原修復(fù)緩沖液(如 Tris/EDTA pH 9.0,枸櫞酸鈉溶液 pH 6.0,等等)
方法
1.按前面描述將切片脫蠟至水。
2.向微波爐專用容器中加入合適的修復(fù)緩沖液(見注意事項(xiàng) 1)
3.從自來(lái)水中取出切片并放入容器中,置于微波爐內(nèi)。如果用家用微波爐,就將之開到最大功率至開始沸騰并煮沸 20 分鐘。如
果采用科研 專用微波爐,就將溫度設(shè)置在 98°C 維持 20 分鐘以修復(fù)抗原(見注意事項(xiàng) 2)。
4.20 分鐘后,取出容器放置水中冷卻 10 分鐘。小心熱溶液(見注意事項(xiàng) 3)。
5.參照手冊(cè)繼續(xù)染色。
注意事項(xiàng)
1.使用非密封的容器,要確保修復(fù)緩沖液足以浸沒(méi)切片幾厘米,防止在煮沸過(guò)程中切片變干。
2.20 分鐘只是抗原修復(fù)的建議時(shí)間。低于 20 分鐘可能會(huì)使修復(fù)不徹底,導(dǎo)致染色較弱。而超過(guò) 20 分鐘可能會(huì)使修復(fù)過(guò)度,導(dǎo)致非特異性 的背景染色,同時(shí)會(huì)增加組織切片從玻片上解離的幾率。因此需要做對(duì)照試驗(yàn),同樣的組織切片分別修復(fù) 5、10、15、20、25、30 分鐘 后開始染色,針對(duì)特異抗體選擇最佳修復(fù)時(shí)間。
3.確保玻片徹底冷卻可以便于下一部操作,而且使抗原表位在經(jīng)歷高溫后復(fù)原。
c) 蒸煮鍋法
許多實(shí)驗(yàn)室使用蒸煮鍋或電飯煲加熱。此方法與微波法相似,都是將緩沖液溫度維持在 100°C,不同之處在于沸騰時(shí)此方法沒(méi)有微波法反應(yīng) 激烈。該方法也可用 100°C 水浴代替。
玻片要置于塑料或金屬架子容器內(nèi),玻璃架和玻璃容器在加熱時(shí)會(huì)破裂。
材料和試劑
蒸煮鍋
玻片放置架及容器(容量大約 400-500ml,如果采用 Tissue –Tek 容器大約 250ml)
抗原修復(fù)緩沖液(如 Tris/EDTA pH 9.0,枸櫞酸鈉溶液 pH 6.0,等等)
方法
1.按前面描述將切片脫蠟至水。
2.依據(jù)用戶手冊(cè)設(shè)置蒸煮鍋并預(yù)熱。
3.在燒瓶中加熱適量修復(fù)緩沖液并煮沸(用微波爐加熱會(huì)更方便)。
4.將盛放玻片架的容器放置蒸煮鍋中。
5.將熱修復(fù)緩沖液小心加到容器中,然后放入玻片架。也可以采用更簡(jiǎn)捷的操作,先向容器中加熱修復(fù)緩沖液再放入蒸煮鍋中。
6.加蓋。盛放緩沖液的容器也須配備蓋子。剛開始時(shí)玻片架可能會(huì)使修復(fù)溶液溫度降低,但幾分鐘內(nèi)會(huì)回升到 95-100°C 之間。
7.達(dá)到溫度后維持 20 分鐘。(見微波法注意事項(xiàng) 1)
8.20 分鐘后,取出容器放置水中冷卻 10 分鐘。熱溶液使用注意事項(xiàng)(見微波法注意事項(xiàng) 2)。
9.依據(jù)手冊(cè)開始組織染色。
3.酶解抗原修復(fù)法
依據(jù)抗體數(shù)據(jù)表中選擇需要的酶。如果沒(méi)有,那么胰蛋白酶適用于大多數(shù)福爾馬林/PFA 固定后需要修復(fù)的抗原。至少有兩種將酶溶液加到組織上的方法:直接用吸管將酶溶液滴加到玻片的組織上或?qū)⒔M織玻片放入酶溶液中。第一種方法反應(yīng)試劑需要量 少,但是因?yàn)槊總€(gè)玻片需要分別處理,較不容易保證孵育時(shí)間的一致。鑒于此,在處理大批量玻片(如數(shù)量>5)時(shí),采用第二種方法較容易。 如果采用全自動(dòng)染色系統(tǒng)(如 Ventana),要查閱酶解修復(fù)操作指南。
a) 滴管法
材料和試劑
37°C 孵育箱
加濕器(恒溫箱自帶或在容器內(nèi)放入濕紙巾)
兩個(gè)盛 TBS 的玻片架容器(TBS 配方詳見緩沖液部分第 71 頁(yè))
酶解抗原修復(fù)溶液(胰蛋白酶如下所述,胃蛋白酶和蛋白酶K見緩沖液部分第71頁(yè))
下面介紹一下胰蛋白酶法。有市售已優(yōu)化的 IHC 用胰蛋白酶產(chǎn)品(Abcam,貨號(hào) ID ab970),也可以按照第 11 章 71 頁(yè)緩沖液部分制備。
方法
1.將胰蛋白酶預(yù)熱至 37°C。小心的將組織切片周圍的水吸干,然后吸取酶溶液滴加到切片上(一般 50-100μl 即可)。用吸管尖端將酶溶液 鋪蓋住整個(gè)切片,注意不要弄壞組織。
2.將玻片置于加濕器內(nèi),然后 37°C 孵育。避免直接將玻片放入恒溫箱架子上,否則會(huì)因溫度不均影響染色質(zhì)量。盛放玻片的容
器最好先預(yù) 熱再放入恒溫箱內(nèi)。
3.10-20 分鐘(需要優(yōu)化)后,取出玻片,流水沖洗 3 分鐘。
4.參照手冊(cè)繼續(xù)染色。
b) 浸泡法
材料和試劑
37°C 水浴
玻片架及玻片架容器
酶解抗原修復(fù)溶液(胰蛋白酶見滴加作用液法,胃蛋白酶和蛋白酶 K 見緩沖液部分第 71 頁(yè))
方法
1.將水浴溫度設(shè)置為酶最適宜的溫度。向盛放玻片架的兩個(gè)容器中加入超純水。容器放入水浴中加熱。(見注意事項(xiàng) 2)
2.按上述方法將切片脫蠟至水后放入水浴箱其中一個(gè)容器中加熱。(見注意事項(xiàng) 3)
3.用水浴箱中另一個(gè)容器中的熱水制備酶解抗原修復(fù)緩沖液,然后將盛有緩沖液的容器放回水浴箱中重新加熱。(見注意事項(xiàng) 4)
4.將加熱過(guò)的玻片放入酶溶液中 10-20 分鐘(見注意事項(xiàng) 5)并間歇緩慢震蕩。取出玻片在流水下沖洗3分鐘,將酶漂洗干凈。
5.參照手冊(cè)繼續(xù)染色。
注意事項(xiàng)
1.仔細(xì)閱讀酶使用手冊(cè),因?yàn)橛行┟感枰厥獾木彌_溶液和活性輔助因子。
2.水或緩沖液的體積要足夠沒(méi)過(guò)玻片。
3.若將冷玻片直接放入酶溶液中會(huì)使溶液溫度降低從而酶活性降低,導(dǎo)致抗原位點(diǎn)修復(fù)不徹底。
4.盡可能快的準(zhǔn)備出抗原修復(fù)緩沖液以避免妨礙酶活性的發(fā)揮。放入玻片之前使溶液達(dá)到需要的溫度。
5.10-20 分鐘只是孵育的建議時(shí)間。低于 10 分鐘可能會(huì)使修復(fù)不徹底,導(dǎo)致染色較弱。而超過(guò) 20 分鐘可能會(huì)使修復(fù)過(guò)度,導(dǎo)致非特異性背 景染色,增加切片從玻片上解離的幾率,損壞組織形態(tài)。因此需要先做對(duì)照試驗(yàn),同樣的組織切片分別孵育 10、15、20、25、30 分鐘后 開始染色,針對(duì)特異抗體尋找到最佳修復(fù)時(shí)間。
免疫組織化學(xué)染色和檢測(cè)實(shí)驗(yàn)方案
1.一般原則
下面的操作適用于沒(méi)有全自動(dòng)染色機(jī)或 capillary gap system 等的實(shí)驗(yàn)室(如Shandon Sequenza)。可用吸管人工加試劑,該手冊(cè)也適用于 全自動(dòng)或半自動(dòng)系統(tǒng)。
培養(yǎng)箱應(yīng)配備有加濕器避免組織變干。變干發(fā)生在任何階段最后都會(huì)導(dǎo)致非特異性染色及高背景染色。帶密封蓋的淺塑料盒,底部鋪上濕紙 巾就是一個(gè)加濕裝置。玻片只要不貼聚紙巾且平放就不會(huì)變干,一個(gè)好的解決辦法就是,將一根塑料輸液管切割成若干適合恒溫箱的小段, 用膠兩個(gè)兩個(gè)的粘到恒溫箱底部,每對(duì)管之間間隔 4cm,這樣能給玻片一個(gè)平穩(wěn)及升起的小平臺(tái),使玻片直接接觸濕紙巾。
一抗和二抗的最佳稀釋度可以從數(shù)據(jù)表中找到,或者通過(guò)試驗(yàn)獲得。根據(jù)所獲得的結(jié)果調(diào)節(jié)至最佳稀釋度。要嚴(yán)格遵照說(shuō)明書中的孵育時(shí)間。
酶解法中,辣根過(guò)氧化物酶 (HRP) 和堿性磷酸酶 (AP) 是最為常用的酶。這些酶有許多底物。
2.操作步驟
緩沖液配方,若需要可在開始下面操作之前先進(jìn)行抗原修復(fù)。
第一天
1.如使用 HRP 標(biāo)記二抗檢測(cè),則需要封閉掉內(nèi)源性過(guò)氧化物酶,但我們建議在開始一抗孵育前不予理會(huì)。
2.在含 0.025% Triton X-100 的 TBS 漂洗玻片 2 X 5 分鐘,輕輕震蕩。
3.用含 10% 正常血清、1% BSA 的 TBS 室溫封閉 2 小時(shí)。空干封閉液(不是漂洗),并用紙巾將玻片周圍擦干。
4.一抗用含 1% BSA 的 TBS 稀釋后加到玻片上。
5.4°C 孵育過(guò)夜。
第二天
1.用含 0.025% Triton X-100 的 TBS 漂洗 2 X 5 分鐘,并輕輕震蕩。
2.如使用 HRP 標(biāo)記二抗檢測(cè),則需將玻片在含 0.3% H2O2 的 TBS 中孵育 15 分鐘 以封閉內(nèi)源性過(guò)氧化物酶。
3.酶法檢測(cè)(HRP 或 AP 標(biāo)記二抗):
參照廠家推薦的稀釋度,用含 1% BSA 的 TBS 稀釋酶標(biāo)二抗,加到玻片上后室溫孵育 1 小時(shí)。
熒光檢測(cè):
參照廠家推薦的稀釋度,用含 1% BSA 的 TBS 稀釋熒光標(biāo)記的二抗,加到玻片上后室溫孵育 1 小時(shí)。此步應(yīng)在暗處進(jìn)行,防止熒光衰退。
4.在 TBS 中漂洗 3 X 5 分鐘。
如采用熒光檢測(cè),則結(jié)束此步后就可以用封固劑和蓋玻片進(jìn)行封固了。
如采用底物顯色,則還需繼續(xù)進(jìn)行下述操作。
5.室溫下與底物作用 10 分鐘。
6.流水沖洗 5 分鐘。
7.復(fù)染(如果需要)。
8.脫水,擦干并封固。
3.對(duì)照
為了評(píng)價(jià)非特異性交叉反應(yīng)和 Fc 受體結(jié)合的影響,與一抗同型但不相關(guān)的抗體(如 BrdU)將來(lái)用做對(duì)照。與不相關(guān)抗原結(jié)合的抗體稱為同 型對(duì)照。對(duì)于全血清抗體而言,對(duì)照抗體是來(lái)源于同種動(dòng)物的未免疫正常血清。
如果沒(méi)有同型對(duì)照,陰性對(duì)照也可,就是用抗體稀釋液代替一抗。強(qiáng)力推薦陽(yáng)性組織對(duì)照,確保抗體達(dá)到預(yù)期效果。根據(jù)實(shí)驗(yàn)需要,也可設(shè) 陰性組織對(duì)照,在該組織中應(yīng)沒(méi)有目標(biāo)蛋白存在的。
使用含 0.025% Triton X-100 的 TBS 有助于降低表面張力,從而使反應(yīng)試劑能更易覆蓋住整個(gè)組織切片。
同時(shí)也能融解 Fc 受體從而減少非特異結(jié)合。Abcam 推薦使用 TBS,它比 PBS 的背景染色更干凈。
注意事項(xiàng):
1.二抗可能會(huì)與組織內(nèi)的內(nèi)源性免疫球蛋白發(fā)生交叉反應(yīng)。以二抗同種動(dòng)物來(lái)源的正常血清預(yù)處理組織,可減少這種作用。加一抗前先與正 常血清孵育從而消除 Fc 受體與一抗和二抗結(jié)合。抗體稀釋緩沖液中的 BSA 能降低疏水作用引起的非特異結(jié)合。
如果組織樣品經(jīng)醛類如甲醛、多聚甲醛、戊二醛等固定后用免疫熒光法 (IF) 檢測(cè),在加一抗之前要用含 0.3M 甘氨酸的封閉液封閉。因?yàn)楦?氨酸能結(jié)合自由醛基,否則這些醛基會(huì)與一抗和二抗結(jié)合造成高背景染色。使用多聚甲醛或戊二醛固定時(shí),由自由醛基導(dǎo)致的高背景很有 可能發(fā)生。
2.一抗應(yīng)稀釋到廠家推薦的最佳稀釋度或者曾經(jīng)篩選到的最佳稀釋度。如果沒(méi)有起始稀釋倍數(shù),我們建議按下述操作。大多數(shù) IHC-P用抗體 的使用濃度在 0.5-10μg/ml 之間。要確保一抗和被染色的組織來(lái)自不同物種。例如,小鼠組織,一抗來(lái)自小鼠,抗鼠 IgG二抗會(huì)與小鼠組 織中的所有內(nèi)源性 IgG 結(jié)合,導(dǎo)致高背景染色。將小鼠單克隆抗體用于小鼠組織將在我們小鼠-對(duì)-小鼠部分中討論。
3.過(guò)夜孵育可以使低親和力的抗體有較長(zhǎng)的時(shí)間結(jié)合到抗原上。然而,不管抗體親和力的高低,一旦抗原抗體結(jié)合達(dá)到飽和或平衡,就不會(huì) 再發(fā)生結(jié)合。因此,過(guò)夜孵育確保了結(jié)合達(dá)到平衡。
4.過(guò)氧化氫 (H2O2) 能抑制內(nèi)源性過(guò)氧化物酶活性從而降低背景染色。檢測(cè)是否存在內(nèi)源性過(guò)氧化物酶,在 DAB (3,3’二氨基鄰苯胺底物)溶液 中水解后孵育組織玻片。如果切片在顯微鏡下出現(xiàn)棕色區(qū)域,說(shuō)明存在過(guò)氧化物酶,因此應(yīng)該做封閉。一些表位被過(guò)氧化物修飾了,降低 了抗原抗體的結(jié)合。初步孵育后再將切片與過(guò)氧化物孵育就能避免此問(wèn)題。
用 TBS 或水稀釋過(guò)氧化氫。有些實(shí)驗(yàn)室用甲醇稀釋,甲醇更適合于血涂片或其它富含過(guò)氧化物酶的組織如肝臟。甲醇稀釋過(guò)氧化氫可減 少水溶液對(duì)組織的損壞。對(duì)于其它組織,我們建議使用 TBS 或水。甲醇/過(guò)氧化物孵育后會(huì)降低一些抗原抗體的結(jié)合,特別是對(duì)于細(xì)胞表 面蛋白來(lái)說(shuō)。內(nèi)源性過(guò)氧化物酶的封閉只用于過(guò)氧化物酶標(biāo)記物如 HRP。
5.酶聯(lián)底物產(chǎn)生有色沉著。最終產(chǎn)生什么樣的有色沉著取決于用什么酶標(biāo)簽以及采用水溶性封片劑還是有機(jī)溶劑封片劑。下面所列的是一些 常用底物:
酶 | 底物 | 顏色 | 優(yōu)點(diǎn) | 缺點(diǎn) | Abcam ID |
辣根過(guò)氧化物酶 (HRP) | 3,3’二氨基鄰苯胺 (DAB) | 棕褐色 | 色澤鮮亮;持久 | 持久 組織中內(nèi)源性過(guò)氧化物酶活性會(huì)造成假陽(yáng)性; AEC 溶于醇類但不溶于有機(jī)介質(zhì) | ab675 |
3-氨基-9-乙基卡巴唑 (AEC) | 紅色 | 色澤鮮亮;藍(lán)紅對(duì) 比鮮明的雙染色 | |||
堿性磷酸酶 (AP) | 5-溴-4-氯-3-吲哚磷酸 酯; | 藍(lán)色 | 色澤鮮亮; | 組織中內(nèi)源性堿性磷酸酶活性會(huì)造成假陽(yáng)性 | ab7413 ab7468 |
硝基四氮唑鹽 (BCIP/NBT)載體藍(lán) | 藍(lán)色 | 色澤較差但是雙色 對(duì)比更鮮明 | |||
葡萄糖氧化酶 | 硝基四氮唑鹽(NBT) | 藍(lán)色 | 無(wú)內(nèi)源性酶活性 | 染色淺(需較高濃度的一抗和二抗?jié)舛龋?/p> |
6.觀察組織和細(xì)胞形態(tài)的復(fù)染劑通常是蘇木精(藍(lán)色)、核固紅或甲基綠。采用熒光檢測(cè)法時(shí),復(fù)染用 DAPI(藍(lán)色)或碘化吡/PI(紅色)。
7.切記 DAB 是一種致癌物,操作時(shí)要穿上防護(hù)服。與次氯酸鈉在密封容器中過(guò)夜可弱化它的致癌作用(相互作用產(chǎn)生有害氣體),再根據(jù) 實(shí)驗(yàn)室操作規(guī)程處理。如果使用 AP,取 0.24mg/ml 的左旋四咪唑加到染料溶液中,來(lái)抑制內(nèi)源性磷酸酶的活性從而降低背景染色。
8.如果使用AEC、固紅、INT 或其它水溶性染料,切記它們?nèi)苡诖碱惾軇┲小Rx用合適的水溶性封片劑。切勿進(jìn)行下述步驟 9中的脫水擦干。
9.通過(guò)再水化使切片脫水并擦干其上的 DAB、新品紅、NBT、TVega 紅、NBT 或其它有機(jī)染料。按照再水化操作步驟的反向操作。
10.將玻片置于 50% 乙醇中 3 分鐘。
11.70% 乙醇 3 分鐘。
12.95% 乙醇 3 分鐘。
13.100% 乙醇 3 分鐘。
14.二甲苯與無(wú)水乙醇 1:1 混合液 3 分鐘。
15.二甲苯 2 X 3 分鐘。
在適當(dāng)?shù)挠袡C(jī)封固液中封固切片。在有機(jī)封固液中封固切片比在水溶性封固液中封固得到的折射率更好。在顯微鏡下看到的圖像更
清晰明顯。
4.信號(hào)放大
為得到一個(gè)較強(qiáng)的信號(hào),有多種策略可以添加更多的酶或熒光染料。
a) 親和素—生物素(ABC)
該技術(shù)是由 Su-Ming Hsu 及其同事 (J Histochem Cytochem. 1981 Apr 29 (4):577-80) 共同建立的。親和素是在雞蛋白中發(fā)現(xiàn)的,親和力高 ,有4個(gè)不可逆的生物素結(jié)合位點(diǎn),并且這種結(jié)合是不可逆的。生物素是羧基化反應(yīng)中酶的輔助因子。
簡(jiǎn)言之,先將一抗結(jié)合到靶蛋白上,再將生物素標(biāo)記二抗結(jié)合到一抗上。另一反應(yīng)系統(tǒng)中,將親和素與生物素化的酶按一定比例混合形成親和素—生物素—酶復(fù)合物,使親和素上保留一定的未結(jié)合位點(diǎn)。切片與抗體孵育后再與此復(fù)合物共同孵育,使復(fù)合物親和素上未結(jié)合位點(diǎn)與 生物素化的二抗結(jié)合,相比較酶標(biāo)二抗或一抗而言可以使更多的酶接觸到底物。
親和素—生物素復(fù)合物有市售的試劑盒,提供有兩種試劑及結(jié)合最佳比例的操作說(shuō)明。該復(fù)合物適用于 Abcam 的任何生物素化的抗體。如果組織中存在有內(nèi)源性的生物素,如腎臟、肝臟、大腦、前列腺、結(jié)腸、腸、睪丸等會(huì)與親和素—生物素復(fù)合物結(jié)合導(dǎo)致背景染色 (Wang and Pevsner, Cell Tissue Res. 1999 Jun;296(3):511-6.)。Abcam提供有抑制這種結(jié)合的試劑盒,產(chǎn)品編號(hào)是 ab3387。
b) 標(biāo)記的鏈霉生物素 (LSAB)
該方法同 ABC 法相似,它利用了鏈霉親和素(親和力與卵白素相似)和生物素之間的相互作用。一抗與生物素標(biāo)記的抗 Ig 二抗結(jié)合后,再 與結(jié)合在酶或熒光染料上的鏈霉親和素結(jié)合。Abcam 提供有鏈霉親和素 — HRP 結(jié)合物,產(chǎn)品編號(hào)是 ab7403。
應(yīng)用鏈霉親和素代替生物素可以減少非特異性背景染色,因?yàn)殒溍褂H和素是非糖基化的,(卵白素不是),因此它不會(huì)與凝集素或其它糖結(jié) 合蛋白反應(yīng)。而且 LSAB 法比 ABC 法靈敏 4—8 倍(詳見 Giorno R, Diagno Immunol. 1984;2(3):161-6)。
c) HRP 聚合物
將二抗與聚合物-酶復(fù)合物結(jié)合形成的新型聚合物-酶-抗體產(chǎn)物(如抗鼠和/或兔 IgG)優(yōu)于卵白素—生物素 (ABC) 和標(biāo)記的鏈霉生物素 (LSAB)。 因?yàn)榇朔N方法比上述兩種方法減少一步,從而免除了內(nèi)源性生物素的干擾。Abcam 提供有羊抗兔/鼠 IgG HRP 多聚物,產(chǎn)品編號(hào)是 ab2891。
d) 直接酪胺信號(hào)放大法 (TSE)
信號(hào)擴(kuò)大最有效的方法之一是 TSE,受專利保護(hù)(又稱 TSA 或 CSA,不同廠家的試劑盒標(biāo)示不一樣),特別適用于其它檢測(cè)系統(tǒng)難以檢測(cè) 到的相對(duì)稀少的抗原,并且可以增強(qiáng)結(jié)合力弱的抗體的反應(yīng)結(jié)果。
此方法是一抗和 HRP 標(biāo)記二抗結(jié)合后利用過(guò)氧化物酶的催化作用,使酪胺蛋白中酪胺部分與抗體共價(jià)結(jié)合。即使在處理玻片清洗抗體時(shí), 共價(jià)結(jié)合的蛋白也不會(huì)被洗掉,因?yàn)槔野锋I是共價(jià)的。將酶或熒光染料標(biāo)記抗體直接結(jié)合到酪胺蛋白結(jié)合物的蛋白部分,就可以獲得信號(hào)。 市售的試劑盒中蛋白是生物素,應(yīng)用的是鏈霉親和素標(biāo)記酶而不是抗體結(jié)合物。此方法的缺點(diǎn)是試劑盒昂貴,且步驟多時(shí)間長(zhǎng)。

微信掃碼在線客服