PRODUCT CENTER
特色產(chǎn)品當(dāng)前位置:首頁(yè) > 特色產(chǎn)品
心肌肌球蛋白是從牛心組織中純化的(1, 2)。完整的肌球蛋白包括其必需輕鏈(ELC)和調(diào)節(jié)輕鏈(RLC)被純化,詳見(jiàn)圖1和圖2。隨后,肌球蛋白通過(guò)α-胰蛋白酶消化,釋放出可溶性的亞片段-1(S1)結(jié)構(gòu)域,并通過(guò)離心分離(3)。純化的肌球蛋白S1片段已在F-肌動(dòng)蛋白激活的ATP酶活性測(cè)定中被證實(shí)具有生物學(xué)活性(見(jiàn)生物學(xué)活性測(cè)定)。牛心肌肌球蛋白S1片段以白色凍干粉形式提供。
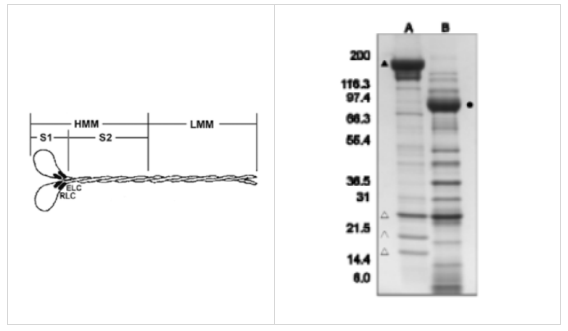
圖1. 肌球蛋白蛋白及其亞片段的示意圖
圖例:肌球蛋白是一種由兩條重鏈和兩條輕鏈組成的六聚體蛋白。在鎂存在的情況下,肌球蛋白可以通過(guò)α-胰蛋白酶被蛋白酶解為重鏈肌球蛋白(HMM)和輕鏈肌球蛋白(LMM)。然而,在EDTA存在的情況下,α-胰蛋白酶會(huì)產(chǎn)生可溶性的肌球蛋白S1片段(3)。
圖2. 完整肌球蛋白和S1肌球蛋白
將20微克的完整牛心肌球蛋白(泳道A)和相應(yīng)的S1肌球蛋白(泳道B)通過(guò)4-20% SDS-PAGE凝膠電泳分離,并用考馬斯亮藍(lán)染色。箭頭表示肌球蛋白重鏈(約200 kDa),箭頭表示調(diào)節(jié)輕鏈(約20 kDa)和兩種必需輕鏈同工型(約25 kDa和21 kDa)。蛋白定量采用Precision Red?蛋白測(cè)定試劑(貨號(hào):ADV02)進(jìn)行。Mark12分子量標(biāo)記來(lái)自Invitrogen。
艾美捷肌球蛋白S1片段(心臟),牛心臟(#CS-MYS03)用途:
1. 測(cè)量鈣激活的肌球蛋白ATP酶活性,當(dāng)其與細(xì)絲結(jié)合時(shí)。
2. 識(shí)別/表征影響TT復(fù)合物調(diào)節(jié)和肌球蛋白ATP酶活性的蛋白質(zhì)或小分子。
3. 識(shí)別/表征影響肌球蛋白/F-肌動(dòng)蛋白相互作用的蛋白質(zhì)或小分子。
儲(chǔ)存與復(fù)溶
短暫離心以使產(chǎn)品聚集在管底。用300微升Milli-Q水復(fù)溶1毫克的MYS03(10毫克瓶用3毫升)將產(chǎn)生濃度為3.3毫克/毫升的心肌S1肌球蛋白溶液,其緩沖液組成為:20 mM PIPES,pH 7.0,5%(質(zhì)量/體積)蔗糖和1%(質(zhì)量/體積)葡聚糖。該蛋白應(yīng)避免反復(fù)凍融。凍干蛋白在4°C干燥條件下(濕度<10%)可穩(wěn)定保存1年。
純度
通過(guò)掃描密度法對(duì)4-20%梯度聚丙烯酰胺凝膠上考馬斯亮藍(lán)染色的蛋白進(jìn)行分析,確定用于產(chǎn)生肌球蛋白S1片段的肌球蛋白及其輕鏈的純度為90%(見(jiàn)圖2)。
生物學(xué)活性測(cè)定 :
牛心肌球蛋白S1片段的生物學(xué)活性可通過(guò)其F-肌動(dòng)蛋白激活的ATP水解速率來(lái)確定。測(cè)定方法是先將肌動(dòng)蛋白聚合形成F-肌動(dòng)蛋白,然后將心肌原肌球蛋白/原肌鈣蛋白復(fù)合物(TT復(fù)合物)與肌動(dòng)蛋白絲按化學(xué)計(jì)量比混合。這會(huì)形成類(lèi)似肌肉纖維細(xì)絲的包被絲。肌球蛋白以亞化學(xué)計(jì)量比加入,并用ATP和鈣啟動(dòng)反應(yīng)。嚴(yán)格的質(zhì)量控制確保在缺乏鈣的情況下,TT復(fù)合物完全抑制肌球蛋白ATP酶活性。加入10微摩爾鈣后,肌球蛋白ATP酶活性將恢復(fù)。鈣與原肌鈣蛋白C結(jié)合,使其從F-肌動(dòng)蛋白上解離,從而使肌球蛋白能夠結(jié)合。
試劑
1. 心肌TT復(fù)合物(1×1毫克,貨號(hào):TT05)
2. 心肌肌球蛋白S1(0.25毫克),貨號(hào):MYS03)
3. 心肌肌動(dòng)蛋白(1毫克,貨號(hào):AD99-A)
4. ATP酶活性生化試劑盒(貨號(hào):BK051)
5. 100 mM ATP,溶于50 mM Tris-HCl,pH 7.5(100微升)
6. 1 M二硫蘇糖醇,溶于水(100微升)
7. PM12反應(yīng)緩沖液(12 mM PIPES-KOH,pH 7.0,2 mM MgCl?)
8. 500 mM EGTA-Na,pH 8.0
肌球蛋白S1片段(心臟),牛心臟文獻(xiàn)參考:
1. Pollard, T.D., . 1982. Methods in Cell Biol. 24:333
2. Margossian, S.S., and Lowey, S. 1982. Methods in Enzymology.85:55-71.
3. Weeds, A.G., and Taylor, R.S. 1975. Nature (London) 257:54.
4. M.J. Holroyde et al. 1980. The calcium and magnesium binding sites on cardiac troponin their role in the regulation of myofibrillar adenosine triphosphatase.

微信掃碼在線客服